Nove publikacije
Identificiran ključni protein koji sprječava gubitak koštane mase kod osteoporoze
Posljednji pregledao: 02.07.2025

Svi iLive sadržaji medicinski se pregledavaju ili provjeravaju kako bi se osigurala što je moguće točnija činjenica.
Imamo stroge smjernice za pronalaženje izvora i samo povezujemo s uglednim medijskim stranicama, akademskim istraživačkim institucijama i, kad god je to moguće, medicinski pregledanim studijama. Imajte na umu da su brojevi u zagradama ([1], [2], itd.) Poveznice koje se mogu kliknuti na ove studije.
Ako smatrate da je bilo koji od naših sadržaja netočan, zastario ili na neki drugi način upitan, odaberite ga i pritisnite Ctrl + Enter.
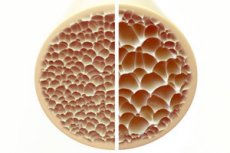
Osteoporoza, stanje karakterizirano poroznim i krhkim kostima, predstavlja značajnu prijetnju zdravlju kostura. Kosti, kao primarna strukturna potpora ljudskog tijela, pružaju vitalnu potporu. Kada se koštana masa smanji, to ne samo da narušava tu potporu, već i narušava cjelokupnu funkciju, što dovodi do smanjene kvalitete života.
Kako se incidencija osteoporoze povećava kod starije populacije, raste i opterećenje zdravstvenih resursa za dugotrajnu skrb. Stoga je potrebno razumjeti mehanizme koji doprinose razvoju osteoporoze i razviti učinkovite ciljane tretmane kako bi se smanjio njezin dugoročni utjecaj.
Osteoblasti i osteoklasti su dvije vrste stanica koje igraju ključnu ulogu u održavanju i pregradnji koštanog tkiva. Dok su osteoblasti stanice koje stvaraju kost i odgovorne su za sintezu i taloženje novog koštanog tkiva, osteoklasti su stanice koje razgrađuju kost i uključene su u razgradnju i uklanjanje starog ili oštećenog koštanog tkiva.
Povećanje udjela osteoklasta dovodi do gubitka koštane mase u stanjima kao što su osteoporoza, reumatoidni artritis (upala zglobova) i koštane metastaze (rak koji se proširio na kosti). Osteoklasti nastaju diferencijacijom makrofaga ili monocita, koji su vrste imunoloških stanica.
Dakle, inhibicija diferencijacije osteoklasta može poslužiti kao terapijska strategija za sprječavanje gubitka koštane mase. Međutim, precizni molekularni mehanizmi koji reguliraju složeni proces pregradnje kostiju ostaju nejasni.
U novoj studiji, profesor Tadayoshi Hayata, g. Takuto Konno i gđa Hitomi Murachi sa Sveučilišta znanosti u Tokiju, zajedno s kolegama, istražili su molekularnu regulaciju diferencijacije osteoklasta. Stimulacija ligandom receptora aktivatora nuklearnog faktora kappa B (RANKL) inducira diferencijaciju makrofaga u osteoklaste.
Osim toga, signalni putevi koštanog morfogenetskog proteina (BMP) i transformirajućeg faktora rasta (TGF)-β uključeni su u regulaciju RANKL-posredovane diferencijacije osteoklasta. U trenutnoj studiji istraživači su imali za cilj istražiti ulogu Ctdnep1, fosfataze (enzima koji uklanja fosfatne skupine) za koju je utvrđeno da potiskuje signalne puteve BMP i TGF-β.
Studija je objavljena u časopisu Biochemical and Biophysical Research Communications.
Profesor Hayata navodi: „RANKL djeluje kao 'akcelerator' za diferencijaciju osteoklasta. Vožnja automobila zahtijeva ne samo gas već i kočnice. Ovdje smo otkrili da Ctdnep1 djeluje kao 'kočnica' u diferencijaciji osteoklasta.“
Istraživači su prvo ispitali ekspresiju Ctdnep1 u mišjim makrofagima tretiranim RANKL-om i netretiranim kontrolnim stanicama. Uočili su da se ekspresija Ctdnep1 nije promijenila kao odgovor na stimulaciju RANKL-om. Međutim, bio je lokaliziran u citoplazmi u granuliranom obliku u makrofagima i diferenciran u osteoklaste, za razliku od njegove normalne perinuklearne lokalizacije u drugim tipovima stanica, što ukazuje na njegovu citoplazmatsku funkciju u diferencijaciji osteoklasta.
Nadalje, smanjenje ekspresije Ctdnep1 (smanjenje ekspresije gena) rezultiralo je povećanjem broja osteoklasta pozitivnih na tartarat-rezistentnu kiselu fosfatazu (TRAP), gdje je TRAP marker diferenciranih osteoklasta.
Izbacivanje Ctdnep1 rezultiralo je povećanom ekspresijom ključnih markera diferencijacije, uključujući "Nfatc1", glavni transkripcijski faktor induciran RANKL-om za diferencijaciju osteoklasta. Ovi rezultati podupiru "kočnu funkciju" Ctdnep1, pri čemu negativno regulira diferencijaciju osteoklasta. Štoviše, izbacivanje Ctdnep1 također je rezultiralo povećanom apsorpcijom kalcijevog fosfata, što sugerira supresivnu ulogu Ctdnep1 u resorpciji kostiju.
Konačno, iako nokautiranje Ctdnep1 nije promijenilo BMP i TGF-β signalizaciju, stanice s nedostatkom Ctdnep1 pokazale su povećane razine fosforiliranih (aktiviranih) proteina, koji su produkti RANKL signalnog puta. Ovi rezultati sugeriraju da inhibitorni učinak Ctdnep1 na diferencijaciju osteoklasta možda nije posredovan BMP i TGF-β signalizacijom, već smanjenjem RANKL signalnog puta i razinama Nfatc1 proteina.
Sveukupno, ovi rezultati pružaju nove uvide u proces diferencijacije osteoklasta i identificiraju potencijalne terapijske ciljeve koji bi se mogli koristiti za razvoj tretmana za smanjenje gubitka koštane mase zbog prekomjerne aktivnosti osteoklasta. Osim bolesti karakteriziranih gubitkom koštane mase, Ctdnep1 je također identificiran kao uzročni faktor meduloblastoma, tumora mozga u djetinjstvu. Autori su optimistični da se njihovo istraživanje može proširiti na druge ljudske bolesti izvan metabolizma kostiju.
Profesor Hayata zaključuje: „Naši rezultati sugeriraju da je Ctdnep1 potreban za sprječavanje prekomjerne osteoklastogeneze. Ovi rezultati mogu dodatno proširiti naše znanje o tome kako mreža fosforilacije-defosforilacije kontrolira diferencijaciju osteoklasta i mogu pružiti nove terapijske strategije za liječenje bolesti kostiju povezanih s prekomjernom aktivnošću osteoklasta.“
