Nove publikacije
Umjetna inteligencija otkriva rak prostate u ranoj fazi koji patolozi propuste
Posljednji pregledao: 23.08.2025

Svi iLive sadržaji medicinski se pregledavaju ili provjeravaju kako bi se osigurala što je moguće točnija činjenica.
Imamo stroge smjernice za pronalaženje izvora i samo povezujemo s uglednim medijskim stranicama, akademskim istraživačkim institucijama i, kad god je to moguće, medicinski pregledanim studijama. Imajte na umu da su brojevi u zagradama ([1], [2], itd.) Poveznice koje se mogu kliknuti na ove studije.
Ako smatrate da je bilo koji od naših sadržaja netočan, zastario ili na neki drugi način upitan, odaberite ga i pritisnite Ctrl + Enter.
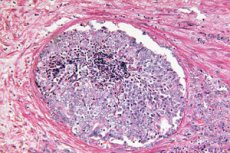
Znanstvena izvješća pokazuju da umjetna inteligencija može prepoznati skrivene morfološke tragove tumora u biopsijama prostate koje je patolog prethodno smatrao benignima. Model dubokog učenja obučen korištenjem slabo nadziranog pristupa predvidio je koji će muškarci s povišenim PSA razviti klinički značajan rak prostate (ISUP > 1) u sljedećih 30 mjeseci, a koji će ostati bez raka najmanje 8 godina. To otvara vrata ranoj stratifikaciji rizika odmah nakon početne „čiste“ biopsije i može pomoći u odlučivanju kome su zaista potrebni ponovljeni invazivni postupci i pojačani nadzor.
Pozadina studije
Primarna biopsija prostate iglom često daje lažno negativne rezultate: značajan udio klinički značajnog raka ostaje „izvan ekrana“, posebno kod tradicionalne sustavne TRUS biopsije. Uvođenje MRI navođenja povećalo je udio otkrivanja klinički značajnog raka i smanjilo broj nepotrebnih ponovljenih postupaka, ali čak i uz moderne strategije, neki agresivni tumori ostaju neotkriveni. Klinička dilema ostaje ista: koga treba promatrati nakon „čiste“ biopsije, a koga treba uputiti na ranu ponovljenu biopsiju, kako se ne bi odgodila dijagnoza i ne bi se pacijenti preopteretili invazivnim intervencijama.
Biološka osnova za rješavanje ovog problema je fenomen TINT-a (tumor-instructed/indicating normal tissue): tumor „rekonfigurira“ okolna naizgled normalna tkiva organa, ostavljajući u njima slabe, ali sustavne tragove - od preoblikovanja strome i hipoksije do metaboličkih promjena. Ove promjene opisane su u eksperimentalnim modelima i kod pacijenata s rakom prostate te koreliraju s agresivnošću tumora, što „normalno“ tkivo čini potencijalnim izvorom dijagnostičkih signala, čak i ako u jezgri biopsije nema očitih kancerogenih žlijezda.
Metode digitalne patologije i dubokog učenja usmjerene su na izdvajanje takvih „suptilnih“ značajki polja iz standardnih H&E presjeka. Za razliku od klasične morfologije, koja se fokusira na očite tumorske strukture, algoritmi mogu uhvatiti distribuirane obrasce u stromi i epitelu povezane s prisutnošću tumora u drugom dijelu organa. To otvara put stratifikaciji rizika odmah nakon negativne biopsije: visok „glass“ rezultat sugerira preporučljivost rane ponovljene biopsije ili vođenja MRI-om, nizak podržava nježnije promatranje.
Ovo je ideja iza nove studije objavljene u časopisu Scientific Reports: autori su testirali može li umjetna inteligencija predvidjeti klinički značajan rak prostate u sljedećih 30 mjeseci na temelju morfoloških znakova iz TINT biopsija. Rad se nadovezuje na prethodno predstavljeni preprint i čini primijenjenu osnovu za implementaciju "terenskih" digitalnih biomarkera u usmjeravanju pacijenata nakon početne "čiste" biopsije.
Kako je to učinjeno: dizajn, podaci, algoritam
Autori su retrospektivno prikupili kohortu od 232 muškarca s povišenim PSA i početnim zaključkom "benigni" na biopsiji iglom (nakon tehničke kontrole, 213 pacijenata i 587 presjeka uključeno je u konačnu analizu; biopsije 1997.-2016., Umea, Švedska). Svaki pacijent je usklađen s "zrcalnim" parom prema dobi, godini dijagnoze i razini PSA: polovica je kasnije dijagnosticirana s rakom prostate (≤30 mjeseci), druga polovica je ostala bez raka najmanje 8 godina. H&E preparati su digitalizirani (20×), izrezani na pločice od 256×256 piksela i uneseni u CLAM (Clustering-constrained Attention Multiple-Instance Learning) - modernu slabo nadziranu shemu, gdje je poznata samo sudbina pacijenta, a ne i oznaka svakog piksela. Značajke su izdvojene pomoću ResNet18 prethodno obučenog na 57 skupova histopatoloških podataka. Krajnja točka je binarna: nizak rizik (benigni/ISUP1) u odnosu na visoki rizik (ISUP2-5).
Točnost predviđanja
U neovisnom testu, model je postigao AUC od 0,81 na svim preparatima i AUC od 0,82 na razini pacijenta. Na pragu koji je pružao prihvatljivu ravnotežu, osjetljivost je bila 0,92 sa stopom lažno pozitivnih od 0,32 (na razini pacijenta). Drugim riječima, među ljudima čija je početna biopsija "promašila", umjetna inteligencija je ispravno označila veliku većinu onih kod kojih je ubrzo potvrđen klinički značajan rak, iako po cijenu nekih lažnih alarma. Za kliniku je ovo signal: "benigni" odgovor na biopsiju ≠ nulti rizik, a može se kvantitativno stratificirati digitalnim staklom.
Što točno umjetna inteligencija "primjećuje" u "normalnom" tkivu?
Interpretacija putem UMAP-a i mapa pažnje pokazala je da su promjene strome najinformativnije:
- Više kolagena u stromi (zbijanje matrice, „fibroza“);
- Manje glatkih mišićnih stanica oko žlijezda;
- Manje uobičajeni su suptilni signali u žljezdanom epitelu, vjerojatno ispod dostupne rezolucije smanjenja uzorkovanja.
Ovaj obrazac uklapa se u koncept TINT-a (tumor-instructed/indicating normal tissue - tumorom instruirano/ukazujuće normalno tkivo): čak se i "norma" u organu gdje je tumor skriven rekonfigurira pod njegovim utjecajem i razlikuje se od "norme" u organu bez tumora. Rak nije samo žarište, već i polje, a umjetna inteligencija uči čitati učinak polja.
Kako je pristup koristan u praksi - potencijalni scenariji
- Ponovna biopsija na temelju rizika: visoka stopa AI na "čistom" staklu - argument u korist rane ponovne biopsije ili vođenja MRI-om umjesto čekanja.
- Personalizacija praćenja: Niska brzina uravnotežuje anksioznost nakon „granične“ magnetske rezonancije i omogućuje umjerenost intenziteta praćenja.
- Trening TINT uzorka: Mape pažnje i interaktivni slojevi pomažu patolozima da vide suptilna polja oko raka, poboljšavajući dosljednost izvješća.
Važno je razumjeti ograničenja
Radi se o jednom centru u sjevernoj Švedskoj (pretežno bijela populacija), dizajn je retrospektivan, početne biopsije su provedene bez MRI navođenja (sustavne TRUS biopsije), a markeri su budući ishodi, a ne "okultni tumor na istom preparatu". Još uvijek nema vanjske validacije u neovisnim centrima/skenerima, niti postoji prospektivno ispitivanje učinka algoritma na kliničke odluke i ishode. Stopa lažno pozitivnih ostaje značajna - model ne zamjenjuje liječnika, ali dodaje probabilistički sloj za zajedničko donošenje odluka.
Što je sljedeće: Plan implementacije
- Višecentrična vanjska validacija (različiti skeneri, protokoli, etničke skupine).
- Prospektivne studije odlučivanja: mijenja li AI skor putanju pacijenta (vrijeme do dijagnoze, broj nepotrebnih ponovljenih biopsija, prekomjerna/nedovoljna dijagnoza).
- Integracija s magnetskom rezonancijom i kliničkim podacima: kombinirani modeli (PSA, MRI PIRADS, klinički faktori + TINT rezultat prema H&E).
- Tehnički koraci: standardizacija digitalizacije, kontrola pomicanja podataka, objašnjivost (preklapanje pažnje za rutinu).
Izvor: Chelebian E., Avenel C., Järemo H., Andersson P., Bergh A., Wählby C., et al. Otkriće tumora koje ukazuje na morfološke promjene u benignim biopsijama prostate putem umjetne inteligencije. Znanstvena izvješća (Nature Portfolio), objavljeno 21. kolovoza 2025. DOI: https://doi.org/10.1038/s41598-025-15105-6
