Medicinski stručnjak članka
Nove publikacije
Liječenje teške sepse i septičkog šoka
Posljednji pregledao: 04.07.2025

Svi iLive sadržaji medicinski se pregledavaju ili provjeravaju kako bi se osigurala što je moguće točnija činjenica.
Imamo stroge smjernice za pronalaženje izvora i samo povezujemo s uglednim medijskim stranicama, akademskim istraživačkim institucijama i, kad god je to moguće, medicinski pregledanim studijama. Imajte na umu da su brojevi u zagradama ([1], [2], itd.) Poveznice koje se mogu kliknuti na ove studije.
Ako smatrate da je bilo koji od naših sadržaja netočan, zastario ili na neki drugi način upitan, odaberite ga i pritisnite Ctrl + Enter.
Učinkovito liječenje sepse moguće je samo uz potpunu kiruršku sanaciju mjesta infekcije i adekvatnu antimikrobnu terapiju. Neadekvatna početna antimikrobna terapija faktor je rizika za smrt kod pacijenata sa sepsom. Održavanje pacijentovog života, sprječavanje i uklanjanje disfunkcija organa mogući su samo uz ciljanu intenzivnu njegu.
Njegov glavni cilj je optimizacija transporta O2 u uvjetima njegove povećane potrošnje, što je tipično za tešku sepsu i septički šok. Ovaj tretman provodi se hemodinamskom i respiratornom potporom.
Hemodinamska podrška
Infuzijska terapija
Infuzijska terapija jedna je od početnih mjera za održavanje hemodinamike i, prije svega, srčanog minutnog volumena. Njezini glavni zadaci kod pacijenata sa sepsom su:
- obnavljanje adekvatne perfuzije tkiva,
- korekcija poremećaja homeostaze,
- normalizacija staničnog metabolizma,
- smanjenje koncentracije medijatora septičke kaskade i toksičnih metabolita.
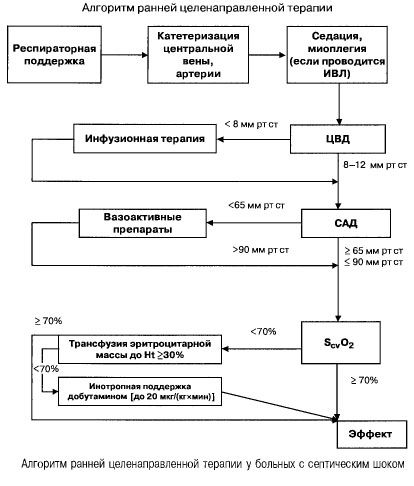
Kod sepse s višestrukim zatajenjem organa i septičkim šokom, pokušavaju se brzo (unutar prvih 6 sati) postići sljedeće vrijednosti važnih pokazatelja:
- hematokrit >30%,
- diureza 0,5 ml/(kgh),
- zasićenost krvi u gornjoj šupljoj veni ili desnom atriju >70%,
- prosječni krvni tlak >65 mm Hg,
- CVP 8-12 mm Hg
Održavanje ovih vrijednosti na navedenoj razini poboljšava preživljavanje pacijenata (kategorija dokaza B). Hemodinamsko praćenje pomoću Swan-Ganz katetera i PICCO tehnologije (transpulmonalna termodilucija i analiza pulsnog vala) proširuje mogućnosti praćenja i procjene učinkovitosti hemodinamske terapije, ali nema dokaza da poboljšavaju preživljavanje.
Optimalna vrijednost predopterećenja odabire se individualno, budući da je potrebno uzeti u obzir stupanj oštećenja endotela i stanje limfne drenaže u plućima, dijastoličku funkciju ventrikula i promjene intratorakalnog tlaka. Volumen infuzijske terapije odabire se tako da PCWP ne prelazi plazmatski COP (sprečavanje OL) i da dođe do povećanja CO. Dodatno se uzimaju u obzir parametri koji karakteriziraju funkciju izmjene plinova u plućima (paO2 i paO2 / FiO2 ) i promjene na radiografskoj slici.
Za infuzijsku terapiju kao dio ciljanog liječenja sepse i septičkog šoka koriste se kristaloidne i koloidne otopine s gotovo identičnim rezultatima.
Svi infuzijski mediji imaju i prednosti i nedostatke. Danas, s obzirom na rezultate eksperimentalnih i kliničkih studija, nema razloga za preferiranje bilo koje određene vrste.
- Na primjer, za adekvatnu korekciju venskog povratka i razine predopterećenja potrebno je primijeniti volumen kristaloida 2-4 puta veći od volumena koloida, što je povezano s osobitostima distribucije otopine u tijelu. Osim toga, infuzija kristaloida povezana je s većim rizikom od edema tkiva, a njihov hemodinamski učinak je kraći od koloida. Istodobno, kristaloidi su jeftiniji, ne utječu na potencijal koagulacije i ne izazivaju anafilaktoidne reakcije. Na temelju navedenog, kvalitativni sastav infuzijskog programa određuje se ovisno o karakteristikama pacijenta, uzimajući u obzir stupanj hipovolemije, fazu DIC sindroma, prisutnost perifernog edema i koncentraciju albumina u krvnom serumu, težinu akutnog oštećenja pluća.
- Nadomjesci plazme (dekstrani, želatinski pripravci, hidroksietil škrob) indicirani su u slučajevima teškog nedostatka BCC-a. Hidroksietil škrobovi sa stupnjem supstitucije od 200/0,5, 130/0,4 i 130/0,42 imaju potencijalnu prednost u odnosu na dekstrane zbog manjeg rizika od izlaska iz membrane i odsutnosti klinički značajnog učinka na hemostazu.
- Uvođenje albumina u kritičnim stanjima može povećati rizik od smrti. Povećanje COP-a tijekom njegove infuzije je prolazno, a zatim, u uvjetima povećane propusnosti kapilarnog korita (sindrom "kapilarnog curenja"), dolazi do daljnje ekstravazacije albumina. Moguće je da će transfuzija albumina biti korisna samo ako je njegova koncentracija u serumu manja od 20 g/l i ako nema znakova "curenja" u intersticij.
- Primjena krioplazme indicirana je kod konzumacijske koagulopatije i smanjenog koagulacijskog potencijala krvi.
- Široko rasprostranjena upotreba mase eritrocita donora trebala bi biti ograničena zbog visokog rizika od razvoja raznih komplikacija (APL, anafilaktičke reakcije itd.). Prema većini stručnjaka, minimalna koncentracija hemoglobina u bolesnika s teškom sepsom je 90-100 g/l.
Korekcija hipotenzije
Nizak perfuzijski tlak zahtijeva hitnu aktivaciju lijekova koji povećavaju vaskularni tonus i/ili inotropnu funkciju srca. Dopamin ili norepinefrin su lijekovi prvog izbora za korekciju hipotenzije u bolesnika sa septičkim šokom.
Dopamin (dopmin) u dozi <10 mcg/(kg x min) povećava krvni tlak, prvenstveno povećanjem CO, i ima minimalan učinak na sistemski vaskularni otpor. Pri visokim dozama prevladava njegov α-adrenergički učinak, što dovodi do arterijske vazokonstrikcije, a pri dozi <5 mcg/(kg x min) dopamin stimulira dopaminske receptore bubrežnih, mezenteričnih i koronarnih žila, što dovodi do vazodilatacije, povećane glomerularne filtracije i izlučivanja Na+.
Norepinefrin povećava srednji arterijski tlak i povećava glomerularnu filtraciju. Optimizacija sistemske hemodinamike pod njegovim djelovanjem dovodi do poboljšanja bubrežne funkcije bez upotrebe niskih doza dopamina. Studije posljednjih godina pokazale su da njegova izolirana primjena, u usporedbi s kombinacijom s visokim dozama dopamina, dovodi do statistički značajnog smanjenja smrtnosti.
Adrenalin je adrenergički lijek s najizraženijim hemodinamskim nuspojavama. Ima učinak ovisan o dozi na otkucaje srca, srednji arterijski tlak, minutni volumen srca, funkciju lijeve klijetke te isporuku i potrošnju O2 . Međutim, tahiaritmije, pogoršanje protoka krvi u organima i hiperlaktatemija javljaju se istodobno. Stoga je primjena adrenalina ograničena na slučajeve potpune refraktornosti na druge kateholamine.
Dobutamin je lijek izbora za povećanje isporuke i potrošnje CO i O2 pri normalnom ili povišenom predopterećenju. Zbog svog pretežnog djelovanja na beta1-adrenergičke receptore, učinkovitiji je od dopamina u povećanju tih parametara.
Eksperimentalne studije su pokazale da kateholamini, osim što podržavaju cirkulaciju krvi, mogu regulirati tijek sistemske upale utječući na sintezu ključnih medijatora s udaljenim učinkom. Pod utjecajem adrenalina, dopamina, noradrenalina i dobutamina, aktivirani makrofagi smanjuju sintezu i lučenje TNF-a.
Odabir adrenergičkih sredstava provodi se prema sljedećem algoritmu:
- srčani indeks 3,5-4 l/(min x m² ), SvO² > 70% - dopamin ili norepinefrin,
- srčani indeks <3,5 l/(min x m2 ), SvO2 <70% - dobutamin (ako je sistolički krvni tlak <70 mm Hg - zajedno s norepinefrinom ili dopaminom).
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ]
Respiratorna podrška
Pluća su među prvim ciljnim organima uključenim u patološki proces kod sepse. Akutno respiratorno zatajenje jedna je od vodećih komponenti disfunkcije više organa. Njegove kliničke i laboratorijske manifestacije kod sepse odgovaraju ALI, a s progresijom patološkog procesa - ARDS-u. Indikacije za mehaničku ventilaciju kod teške sepse određuju se ovisno o težini parenhimskog respiratornog zatajenja (ARF ili ARDS). Njezin kriterij je respiratorni indeks:
- <200 - indicirana je trahealna intubacija i respiratorna potpora,
- >200 - očitanja se određuju pojedinačno.
Ako je pacijent pri svijesti tijekom spontanog disanja uz potporu kisikom, nema visokog utroška rada disanja i izražene tahikardije (HR <120 u minuti), normalne vrijednosti venskog povrata SO2 > 90%, tada je moguće odustati od prebacivanja na umjetnu ventilaciju. Međutim, potrebno je pažljivo pratiti stanje pacijenta. Optimalna vrijednost SO2 je oko 90%. Može se održavati različitim metodama isporuke plina (maske za lice, nazalni kateteri) u netoksičnim koncentracijama (FiO2 < 0,6). Neinvazivna umjetna ventilacija kontraindicirana je kod sepse (kategorija dokaza B).
Treba izbjegavati visokovolumenske mehaničke ventilacije (MVV) (VO2 = 12 ml/kg), jer se u takvim slučajevima povećava lučenje citokina iz pluća, što dovodi do pogoršanja MOF-a. Potrebno je pridržavati se koncepta sigurne mehaničke ventilacije, koja je moguća ako su ispunjeni sljedeći uvjeti (kategorija dokaza A):
- rastvoreni kisik <10 ml/kg,
- neinvertirani omjer udisaja i izdisaja,
- vršni tlak u dišnim putovima <35 cm H2O,
- FiO2 <0,6 .
Odabir parametara respiratornog ciklusa provodi se sve dok se ne postigne adekvatna mehanička ventilacija, a kriteriji su paO2 > 60 mm Hg, SpO2 > 88-93%, pvO2 35-45 mm Hg, SvO2 > 55%.
Jedna od učinkovitih metoda za optimizaciju izmjene plinova je provođenje umjetne ventilacije u ležećem položaju (Prone Positioning) (kategorija dokaza B). Ovaj položaj je učinkovit kod pacijenata u najtežem stanju, iako je njegov učinak na smanjenje smrtnosti u dugoročnom razdoblju statistički beznačajan.
Nutritivna podrška
Provođenje umjetne nutritivne potpore važan je element liječenja, jedna od obveznih mjera, budući da je razvoj sindroma višestrukog zatajenja organa kod sepse obično popraćen manifestacijama hipermetabolizma. U takvoj situaciji energetske potrebe zadovoljavaju se uništavanjem vlastitih staničnih struktura (autokanibalizam), što pogoršava disfunkciju organa i povećava endotoksikozu.
Nutritivna potpora smatra se metodom sprječavanja teške iscrpljenosti (nedostatak proteina i energije) na pozadini izraženog povećanja kata- i metabolizma. Uključivanje enteralne prehrane u kompleks intenzivne terapije sprječava kretanje crijevne mikroflore, disbakteriozu, povećava funkcionalnu aktivnost enterocita i zaštitna svojstva crijevne sluznice. Ovi čimbenici smanjuju stupanj endotoksikoze i rizik od sekundarnih infektivnih komplikacija.
Izračun nutritivne potpore:
- energetska vrijednost - 25-35 kcal/(kg tjelesne težine x dan),
- količina proteina - 1,3-2,0 g/(kg tjelesne težine x dan),
- količina ugljikohidrata (glukoze) - manje od 6 g/kg/dan,
- količina masti - 0,5-1 g/kg/dan,
- glutamin dipeptidi 0,3-0,4 g/kg/dan,
- vitamini - standardni dnevni set + vitamin K (10 mg/dan) + vitamini B1 i B6 ( 100 mg/dan) + vitamini A, C, E,
- mikroelementi - standardni dnevni set + Zn (15-20 mg/dan + 10 mg/dan u prisutnosti rijetke stolice),
- elektroliti - Na+, K+, Ca2+ prema izračunima ravnoteže i koncentraciji u plazmi.
Rani početak nutritivne potpore (24-36 sati) učinkovitiji je nego 3.-4. dana intenzivne terapije (kategorija dokaza B), posebno kod enteralne sondne prehrane.
Kod teške sepse nema prednosti enteralne ili parenteralne prehrane; trajanje disfunkcije organa i trajanje respiratorne i inotropne potpore su isti, a stope smrtnosti su iste. S obzirom na navedeno, rana enteralna prehrana je jeftinija alternativa parenteralnoj prehrani. Korištenje smjesa obogaćenih dijetalnim vlaknima (prebiotici) za hranjenje putem sonde značajno smanjuje učestalost proljeva kod pacijenata s teškom sepsom.
Za učinkovitu sintezu proteina u tijelu važno je održavati metabolički omjer "ukupni dušik, g - neproteinske kalorije, kcal" = 1-(110-130). Maksimalna doza ugljikohidrata je 6 g / (kg tjelesne težine dnevno), budući da unošenje velikih doza prijeti hiperglikemijom i aktivacijom katabolizma u skeletnim mišićima. Preporučuje se davanje masnih emulzija non-stop.
Kontraindikacije za nutritivnu potporu:
- dekompenzirana metabolička acidoza,
- individualna netolerancija na nutritivne potporne medije,
- teška neliječena hipovolemija,
- refraktorni šok - doza dopamina >15 mcg/(kg x min) i sistolički krvni tlak <90 mm Hg,
- teška, neizlječiva arterijska hipoksemija.
Glikemijska kontrola
Važan aspekt kompleksnog liječenja teške sepse je stalno praćenje koncentracije glukoze u krvnoj plazmi i inzulinska terapija. Visoka glikemija i potreba za njezinom korekcijom faktori su nepovoljnog ishoda kod sepse. S obzirom na navedene okolnosti, kod pacijenata se održava normoglikemija (4,5-6,1 mmol/l), za što se, kada koncentracija glukoze poraste iznad prihvatljivih vrijednosti, provodi infuzija inzulina (0,5-1 U/h). Ovisno o kliničkoj situaciji, koncentracija glukoze prati se svakih 1-4 sata. Prilikom primjene ovog algoritma zabilježen je statistički značajan porast preživljavanja pacijenata.
 [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ]
[ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ]
Glukokortikoidi
Rezultati suvremenih studija o učinkovitosti upotrebe glukokortikoida kod pacijenata sa septičkim šokom sažeti su u sljedećim tvrdnjama:
- Nije prikladno koristiti hormone u visokim dozama [metilprednizolon 30-120 mg/(kg x dan) jednom ili tijekom 9 dana, deksametazon 2 mg/(kg x dan) tijekom 2 dana, betametazon 1 mg/(kg x dan) tijekom 3 dana] - povećan rizik od bolničkih infekcija, bez utjecaja na preživljavanje,
- Primjena hidrokortizona u dozi od 240-300 mg dnevno tijekom 5-7 dana ubrzava stabilizaciju hemodinamskih parametara, omogućuje prekid vaskularne potpore i poboljšava preživljavanje u bolesnika s istodobnom relativnom adrenalnom insuficijencijom (kategorija dokaza B).
Potrebno je napustiti kaotično empirijsko propisivanje prednizolona i deksametazona - nema osnova za ekstrapolaciju novih informacija na njih. U nedostatku laboratorijskih dokaza relativne adrenalne insuficijencije, primjenjuje se hidrokortizon u dozi od 300 mg dnevno (u 3-6 injekcija).
- u refraktornom šoku,
- ako su potrebne visoke doze vazopresora za održavanje učinkovite hemodinamike.
Moguće je da je u uvjetima sistemske upale u septičkom šoku učinkovitost hidrokortizona povezana s aktivacijom inhibitora nuklearnog faktora kB (NF-kB-a) i korekcijom relativne adrenalne insuficijencije. Zauzvrat, inhibicija aktivnosti transkripcijskog nuklearnog faktora (NF-kB) dovodi do smanjenja stvaranja inducibilne NO sintetaze (NO je najsnažniji endogeni vazodilatator), proinflamatornih citokina, COX i adhezijskih molekula.
Aktivirani protein C
Jedna od karakterističnih manifestacija sepse je poremećaj sistemske koagulacije (aktivacija kaskade koagulacije i inhibicija fibrinolize), što u konačnici dovodi do hipoperfuzije i disfunkcije organa. Učinak aktiviranog proteina C na upalni sustav ostvaruje se na nekoliko načina:
- smanjenje vezanja selektina na leukocite, što štiti endotel od oštećenja, što igra ključnu ulogu u razvoju sistemske upale,
- smanjeno oslobađanje citokina iz monocita,
- blokiranje oslobađanja TNF-a iz leukocita,
- inhibicija proizvodnje trombina (potencira upalni odgovor).
Antikoagulantno, profibrinolitičko i protuupalno djelovanje
- aktivirani protein C je posljedica
- razgradnja faktora Va i VIIIa - supresija stvaranja tromba,
- supresija inhibitora aktivatora plazminogena - aktivacija fibrinolize,
- izravan protuupalni učinak na endotelne stanice i neutrofile,
- zaštita endotela od apoptoze
Primjena aktiviranog proteina C [drotrekogin alfa (aktivirani)] u dozi od 24 mcg/(kg h) tijekom 96 h smanjuje rizik od smrti za 19,4%. Indikacije za primjenu: sepsa s akutnim MOF-om i visokim rizikom od smrti (APACHE II > 25 bodova, disfunkcija 2 ili više organa, kategorija dokaza B).
Aktivirani protein C ne smanjuje smrtnost u djece, pacijenata s disfunkcijom jednog organa, APACHE II < 25 bodova, u pacijenata s nekirurškom sepsom.
 [ 14 ], [ 15 ], [ 16 ], [ 17 ]
[ 14 ], [ 15 ], [ 16 ], [ 17 ]
Imunoglobulini
Preporučljivost intravenske primjene imunoglobulina (IgG i IgG+IgM) povezana je s njihovom sposobnošću ograničavanja prekomjernog djelovanja proinflamatornih citokina, povećanja klirensa endotoksina i stafilokoknog superantigena, uklanjanja anergičnosti i pojačavanja učinka ß-laktamskih antibiotika. Njihova primjena u liječenju teške sepse i septičkog šoka jedina je metoda imunokorekcije koja povećava preživljavanje. Najbolji učinak zabilježen je pri korištenju kombinacije IgG i IgM [RR=0,48 (0,35-0,75), kategorija dokaza A]. Standardni režim doziranja je 3-5 ml/(kg x dan) tijekom 3 dana zaredom. Pri korištenju imunoglobulina, najoptimalniji rezultati postignuti su u ranoj fazi šoka („topli šok“) i kod pacijenata s teškom sepsom (APACHE II rezultat od 20-25 bodova).
Prevencija duboke venske tromboze
Prevencija duboke venske tromboze donjih ekstremiteta značajno utječe na ishode liječenja u bolesnika sa sepsom (kategorija dokaza A). U tu svrhu koriste se i nefrakcionirani i nizkomolekularni heparini. Glavne prednosti heparina niske molekularne težine su manja učestalost hemoragijskih komplikacija, slabiji učinak na funkciju trombocita i dugotrajan učinak (mogu se primjenjivati jednom dnevno).
Sprječavanje nastanka stresnih ulkusa gastrointestinalnog trakta
Ovaj smjer igra značajnu ulogu u povoljnom ishodu liječenja pacijenata s teškom sepsom i septičkim šokom, budući da je stopa smrtnosti od krvarenja iz stresnih ulkusa gastrointestinalnog trakta 64-87%. Bez preventivnih mjera, stresni ulkusi javljaju se kod 52,8% kritično bolesnih pacijenata. Međutim, primjena inhibitora protonske pumpe i blokatora histaminskih H2 receptora smanjuje rizik za više od 2 puta (prva skupina lijekova je učinkovitija od druge). Glavni smjer prevencije i liječenja je održavanje pH unutar 3,5-6,0. Treba naglasiti da osim gore navedenih lijekova, enteralna prehrana igra važnu ulogu u sprječavanju nastanka stresnih ulkusa.
Ekstrakorporalno pročišćavanje krvi
Različite biološki aktivne tvari i metabolički produkti uključeni u razvoj generalizirane upale ciljevi su metoda detoksikacije, što je posebno važno u nedostatku prirodnog hepatorenalnog klirensa u uvjetima zatajenja više organa. Metode nadomjesne bubrežne terapije smatraju se obećavajućima, jer mogu utjecati ne samo na uremijske poremećaje kod pacijenata s bubrežnim zatajenjem, već i pozitivno utjecati na druge promjene homeostaze i disfunkcije organa koje se javljaju kod sepse, šoka i zatajenja više organa.
Do danas nema podataka koji potvrđuju potrebu korištenja ekstrakorporalnih metoda pročišćavanja krvi kao jednog od glavnih smjerova patogenetske terapije sepse i septičkog šoka. Njihova upotreba je opravdana u slučaju višestrukog zatajenja organa s dominacijom bubrega.
 [ 18 ], [ 19 ], [ 20 ], [ 21 ], [ 22 ], [ 23 ]
[ 18 ], [ 19 ], [ 20 ], [ 21 ], [ 22 ], [ 23 ]
Hemodijaliza
Bit metode je difuzija tvari niske molekularne težine (do 5x103 Da ) kroz polupropusnu membranu i uklanjanje viška tekućine iz tijela duž gradijenta tlaka. Hemodijaliza se široko koristi za liječenje pacijenata s kroničnim i akutnim zatajenjem bubrega. Brzina difuzije tvari eksponencijalno ovisi o njihovoj molekularnoj težini. Na primjer, uklanjanje oligopeptida je sporije od njihove sinteze.
Hemofiltracija
Hemofiltracija je učinkovita metoda za uklanjanje tvari molekularne težine od 5x10³ - 5x10⁴ Da i jedini način za uklanjanje velike skupine biološki aktivnih tvari i metabolita iz tijela. Metoda se temelji na konvekcijskoj metodi prijenosa mase. Osim adekvatne korekcije azotemije, hemofiltracija učinkovito uklanja anafilatoksine C3a, C5a, proinflamatorne citokine (TNF-a, IL-1b, 6 i 8), ß2-mikroglobulin, mioglobin, paratireoidni hormon, lizozim (molekularna težina - 6000 Da), a-amilazu (molekularna težina - 36 000-51 000 Da), kreatin fosfokinazu, alkalnu fosfatazu, transaminaze i druge tvari. Hemofiltracija uklanja aminokiseline i proteine plazme (uključujući imunoglobuline i cirkulirajuće imunološke komplekse).
Hemodijafiltracija
Hemodijafiltracija je najmoćnija metoda pročišćavanja krvi, koja kombinira difuziju i konvekciju (tj. GD i GF). Dodatni doprinos procesu detoksikacije daje sorpcija patoloških tvari na membrani filtera.
Plazmafereza
Plazmafereza (izmjena plazme, filtracija plazme) također se smatra mogućom metodom za korekciju generalizirane upale kod pacijenata sa sepsom i septičkim šokom. Optimalnom metodom smatra se primjena izmjene plazme u kontinuiranom načinu rada s uklanjanjem 3-5 volumena plazme i njezinom istovremenom zamjenom svježe smrznutim, albuminskim, koloidnim i kristaloidnim otopinama. S koeficijentom prosijavanja od 1, filtracija plazme osigurava dobro uklanjanje C-reaktivnog proteina, haptoglobina, fragmenta komplementa C3, 1-antitripsina, IL-6, tromboksana-B2, faktora stimulacije granulocita, TNF-a. Korištenje sorbenata za pročišćavanje pacijentove plazme smanjuje rizik od infekcije i smanjuje troškove postupka, budući da nema potrebe za korištenjem stranih proteina.
Primjena produljene infuzije natrijevog selenita (selenaze) 1000 mcg/dan kod teške sepse dovodi do smanjenja smrtnosti.
Selen je esencijalni mikroelement, čija je važnost povezana s njegovom ključnom ulogom u antioksidativnim sustavima stanica. Razina selena u krvi održava se unutar 1,9-3,17 μM/l. Potreba za selenom je 50-200 μg dnevno, a ovisi o dostupnosti drugih antioksidansa i mikroelemenata.
Selen je snažan antioksidans, komponenta glutation peroksidaze, fosfolin glutation peroksidaze, drugih oksidoreduktaza i nekih transferaza. Glutation peroksidaza je najvažnija karika u endogenom antioksidativnom sustavu.
Učinkovitost selena u kritičnim uvjetima proučavana je posljednjih godina. Ta su istraživanja pokazala da su glavni mehanizmi djelovanja selena sljedeći:
- supresija hiperaktivacije NF-kB;
- smanjena aktivacija komplementa;
- njegovo djelovanje kao imunomodulatora, antioksidansa i protuupalnog sredstva
- održavanje iskorištenja peroksida;
- supresija endotelne adhezije (smanjena ekspresija ICAM-1, VCAM-2,
- E - selektin, P - selektin);
- zaštita endotela od oksiradikala (korištenjem selenoproteina P, koji sprječava stvaranje peroksinitrita iz O2 i NO).
Ukratko, možemo definirati specifične zadatke intenzivne njege za tešku sepsu:
- Hemodinamska podrška: CVP 8-12 mm Hg, prosječni krvni tlak >65 mm Hg, diureza 0,5 ml/(kg h), hematokrit >30%, zasićenost miješane venske krvi >70%.
- Vršni tlak u dišnim putovima pri respiratornoj potpori <35 cm H2O, inspiratorni udio kisika <60%, disajni volumen <10 ml/kg, omjer udisaja i izdisaja bez invertiranja.
- Glukokortikoidi - "niske doze" (hidrokortizon 240-300 mg dnevno).
- Aktivirani protein C 24 mcg/(kg h) tijekom 4 dana kod teške sepse (APACHE II >25).
- Imunokorekcijska nadomjesna terapija pentaglobinom.
- Prevencija duboke venske tromboze donjih ekstremiteta.
- Sprječavanje nastanka stresnih ulkusa gastrointestinalnog trakta: primjena inhibitora protonske pumpe i blokatora H2-histaminskih receptora.
- Nadomjesna terapija za akutno zatajenje bubrega.
- Nutritivna potpora: energetska vrijednost hrane 25-30 kcal/kg tjelesne težine x dan), proteini 1,3-2,0 g/(kg tjelesne težine x dan), glutamin dipeptidi 0,3-0,4 g/(kg x dan), glukoza - 30-70% neproteinskih kalorija, uz uvjet da se glikemija održava <6,1 mmol/l, masti - 15-50% neproteinskih kalorija.

