Medicinski stručnjak članka
Nove publikacije
Patogeneza hepatitisa B
Posljednji pregledao: 07.07.2025

Svi iLive sadržaji medicinski se pregledavaju ili provjeravaju kako bi se osigurala što je moguće točnija činjenica.
Imamo stroge smjernice za pronalaženje izvora i samo povezujemo s uglednim medijskim stranicama, akademskim istraživačkim institucijama i, kad god je to moguće, medicinski pregledanim studijama. Imajte na umu da su brojevi u zagradama ([1], [2], itd.) Poveznice koje se mogu kliknuti na ove studije.
Ako smatrate da je bilo koji od naših sadržaja netočan, zastario ili na neki drugi način upitan, odaberite ga i pritisnite Ctrl + Enter.
U patogenezi hepatitisa B može se identificirati nekoliko vodećih karika u patogenetskom lancu:
- unošenje patogena - infekcija;
- fiksacija na hepatocitu i prodiranje u stanicu;
- umnožavanje virusa i njegovo "izbacivanje" na površinu hepatocita, kao i u krv;
- aktivacija imunoloških reakcija usmjerenih na eliminaciju patogena;
- oštećenje organa i sustava imunološkim kompleksima;
- stvaranje imuniteta, oslobađanje od patogena, oporavak.
Budući da se infekcija hepatitisom B uvijek događa parenteralno, može se smatrati da je trenutak infekcije praktički jednak prodiranju virusa u krv. Pokušaji nekih istraživača da razlikuju enteralnu i regionalnu fazu kod hepatitisa B slabo su potkrijepljeni. Postoji više osnova za vjerovanje da virus odmah ulazi u jetru protokom krvi.
Tropizam virusa hepatitisa B prema tkivu jetre unaprijed je određen prisutnošću posebnog receptora u HBsAg - polipeptida molekularne težine od 31 000 Da (P31), koji ima aktivnost vezanja albumina. Slična albuminska zona nalazi se i na membrani hepatocita u jetri ljudi i čimpanza, što u biti određuje tropizam HBV prema jetri ljudi i čimpanza.
Kada virus prodre u hepatocit, oslobađa se virusna DNA koja, ulazeći u jezgru hepatocita i djelujući kao matrica za sintezu nukleinskih kiselina, pokreće niz uzastopnih bioloških reakcija, čiji je rezultat sastavljanje nukleokapside virusa. Nukleokapsida migrira kroz nuklearnu membranu u citoplazmu, gdje se odvija konačno sastavljanje Dane čestica - kompletnog virusa hepatitisa B.
Međutim, treba napomenuti da kada je hepatocit zaražen, proces može teći na dva načina - replikativni i integrativni. U prvom slučaju razvija se slika akutnog ili kroničnog hepatitisa, a u drugom - virusno nošenje.
Razlozi koji određuju dvije vrste interakcije između virusne DNA i hepatocita nisu precizno utvrđeni. Najvjerojatnije je vrsta odgovora genetski određena.
Rezultat replikativne interakcije je sastavljanje osnovnih antigenskih struktura (u jezgri) i sastavljanje kompletnog virusa (u citoplazmi), nakon čega slijedi prezentacija kompletnog virusa ili njegovih antigena na membrani ili u strukturi membrane hepatocita.
Općenito je prihvaćeno da replikacija virusa ne rezultira oštećenjem stanica na razini hepatocita, budući da virus hepatitisa B nema citopatski učinak. Ovaj stav ne može se smatrati nepobitnim, budući da se temelji na eksperimentalnim podacima koji, iako ukazuju na odsutnost citopatskog učinka virusa hepatitisa B, dobiveni su na kulturama tkiva i stoga se ne mogu u potpunosti ekstrapolirati na virusni hepatitis B kod ljudi. U svakom slučaju, pitanje odsutnosti oštećenja hepatocita tijekom replikativne faze zahtijeva dodatna istraživanja.
Međutim, bez obzira na prirodu interakcije virusa sa stanicom, jetra je nužno uključena u imunopatološki proces. U ovom slučaju, oštećenje hepatocita povezano je s činjenicom da se kao rezultat ekspresije virusnih antigena na membrani hepatocita i oslobađanja virusnih antigena u slobodnu cirkulaciju uključuje lanac sekvencijalnih staničnih i humoralnih imunoloških reakcija, čiji je konačni cilj uklanjanje virusa iz tijela. Ovaj proces provodi se u potpunosti u skladu s općim obrascima imunološkog odgovora na virusne infekcije. Za eliminaciju patogena uključuju se stanične citotoksične reakcije, posredovane različitim klasama efektorskih stanica: K stanicama, T stanicama, prirodnim ubojicama, makrofagima. Tijekom tih reakcija, zaraženi hepatociti se uništavaju, što je popraćeno oslobađanjem virusnih antigena (HBcAg, HBeAg, HBsAg), koji pokreću sustav geneze antitijela, uslijed čega se u krvi nakupljaju specifična antitijela, prvenstveno na jezgru - anti-HBc i e-antigen - anti-HBE. Posljedično, oslobađanje jetrene stanice od virusa događa se u procesu njezine smrti zbog reakcija stanične citolize.
Istodobno, specifična antitijela koja se nakupljaju u krvi vežu virusne antigene, tvoreći imunološke komplekse koje fagocitiraju makrofagi i izlučuju bubrezi. U tom slučaju mogu se pojaviti različite lezije imunoloških kompleksa u obliku glomerulonefritisa, arteritisa, artralgije, kožnih osipa itd. Uz sudjelovanje specifičnih antitijela, tijelo se čisti od patogena i dolazi do potpunog oporavka.
U skladu s ocrtanim konceptom patogeneze hepatitisa B, sva raznolikost kliničkih varijanti tijeka bolesti obično se objašnjava osobitostima interakcije virusa i suradnjom imunokompetentnih stanica, drugim riječima, snagom imunološkog odgovora na prisutnost virusnih antigena. Prema suvremenim konceptima, snaga imunološkog odgovora je genetski određena i povezana s antigenima histokompatibilnosti HLA lokusa prve klase.
Općenito je prihvaćeno da se u uvjetima adekvatnog imunološkog odgovora na virusne antigene akutni hepatitis klinički razvija s cikličkim tijekom i potpunim oporavkom. Na pozadini smanjenja imunološkog odgovora na virusne antigene, imunološki posredovana citoliza je neznatno izražena, stoga ne dolazi do učinkovitog uklanjanja zaraženih stanica jetre, što dovodi do blagih kliničkih manifestacija s dugotrajnom perzistencijom virusa i, moguće, razvojem kroničnog hepatitisa. Istodobno, naprotiv, u slučaju genetski određenog snažnog imunološkog odgovora i masivne infekcije (hemotransfuzija) nastaju opsežna područja oštećenja stanica jetre, koja klinički odgovaraju teškim i malignim oblicima bolesti.
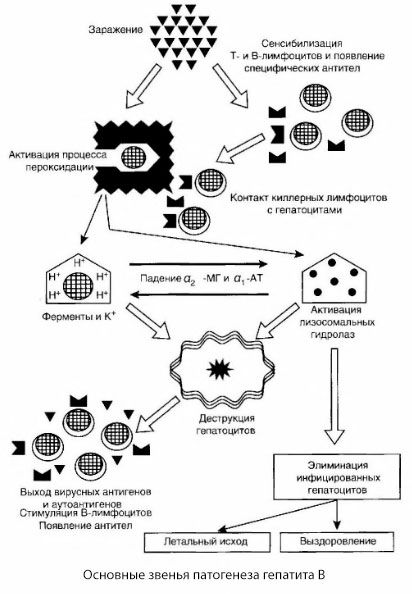
Prikazana shema patogeneze hepatitisa B odlikuje se svojom koherentnošću; međutim, sadrži niz kontroverznih i slabo proučenih točaka.
Ako slijedimo koncept hepatitisa B kao imunopatološke bolesti, mogli bismo očekivati porast staničnih citotoksičnih reakcija s povećanjem težine bolesti. Međutim, u teškim oblicima, indeksi stanične veze imuniteta su oštro smanjeni, uključujući višestruki pad, u usporedbi s onima kod zdrave djece, i indeks citotoksičnosti K-stanica. U malignom obliku, tijekom razdoblja razvoja masivne nekroze jetre, a posebno hepatičke kome, primjećuje se potpuna nemogućnost limfocita za blastnu transformaciju pod utjecajem fitohematutinina, stafilokoknog endotoksina i HBsAg. Osim toga, ne postoji sposobnost leukocita za migraciju prema reakciji inhibicije migracije leukocita (LMIC), a otkriveno je naglo povećanje propusnosti membrana limfocita prema rezultatima njihovih studija korištenjem fluorescentne tetraciklinske sonde.
Dakle, ako su indeksi fluorescencije limfocita kod zdravih osoba 9,9±2%, a kod tipičnog hepatitisa B s benignim tijekom povećavaju se na 22,3±2,7%, tada kod malignih oblika broj fluorescentnih limfocita doseže prosječno 63,5±5,8%. Budući da se povećanje propusnosti staničnih membrana u literaturi nedvosmisleno procjenjuje kao pouzdan pokazatelj njihove funkcionalne inferiornosti, može se zaključiti da kod hepatitisa B, posebno u malignom obliku, dolazi do grubog oštećenja limfocita. To potvrđuju i indeksi citotoksičnosti K-stanica. U teškom obliku, u 1.-2. tjednu bolesti, citotoksičnost iznosi 15,5±8,8%, a u malignom obliku u 1. tjednu - 6,0±2,6, u 2. - 22,0±6,3% s normom od 44,8±2,6%.
Prikazani podaci jasno ukazuju na izražene poremećaje u staničnoj vezi imuniteta u bolesnika s teškim oblicima hepatitisa B. Također je očito da se te promjene javljaju sekundarno, kao posljedica oštećenja imunokompetentnih stanica toksičnim metabolitima i, moguće, cirkulirajućim imunološkim kompleksima.
Kao što su studije pokazale, kod pacijenata s teškim oblicima hepatitisa B, posebno u slučaju razvoja masivne nekroze jetre, titar HBsAg i HBeAg u krvnom serumu se smanjuje, a istovremeno se počinju detektirati antitijela na površinski antigen u visokim titrima, što je potpuno nekarakteristično za benigne oblike bolesti, kod kojih se anti-HBV pojavljuju tek u 3.-5. mjesecu bolesti.
Brzi nestanak antigena virusa hepatitisa B uz istovremenu pojavu visokih titara antivirusnih antitijela sugerira intenzivno stvaranje imunoloških kompleksa i njihovo moguće sudjelovanje u patogenezi razvoja masivne nekroze jetre.
Dakle, činjenični materijali ne dopuštaju nam nedvosmisleno tumačenje hepatitisa B samo s gledišta imunopatološke agresije. I poanta nije samo u tome da nije pronađena veza između dubine i prevalencije morfoloških promjena u jetri, s jedne strane, i težine faktora stanične imunosti, s druge strane. Teoretski, ova okolnost mogla bi se objasniti kasnim fazama proučavanja pokazatelja stanične imunosti, kada su imunokompetentne stanice bile izložene snažnim toksičnim učincima zbog rastuće funkcionalne insuficijencije jetre. Naravno, može se pretpostaviti da se imunološka citoliza hepatocita događa u najranijim fazama infektivnog procesa, moguće čak i prije pojave kliničkih simptoma teškog oštećenja jetre. Međutim, takva pretpostavka je malo vjerojatna, budući da su slični pokazatelji stanične imunosti otkriveni kod pacijenata s najakutnijim (munjevitim) tijekom bolesti, a osim toga, tijekom morfološkog pregleda tkiva jetre nije otkrivena masivna limfocitna infiltracija, dok su istovremeno otkrivena kontinuirana polja nekrotičnog epitela bez pojava resorpcije i limfocitne agresije.
Vrlo je teško objasniti morfološku sliku akutnog hepatitisa samo s gledišta imunološke stanične citolize, stoga u ranim studijama citotoksični učinak virusa hepatitisa B nije bio isključen.
Trenutno je ova pretpostavka djelomično potvrđena otkrićem virusa hepatitisa B. Kao što su studije pokazale, učestalost otkrivanja markera hepatitisa D izravno ovisi o težini bolesti: u blagim oblicima otkrivaju se u 14%, umjerenim - u 18%, teškim - 30%, a malignim - u 52% pacijenata. S obzirom na to da virus hepatitisa D ima nekrozogeni citopatogeni učinak, može se smatrati utvrđenim da je koinfekcija virusima hepatitisa B i D od velike važnosti u razvoju fulminantnih oblika hepatitisa B.
Patogeneza hepatitisa B može se prikazati na sljedeći način. Nakon prodiranja virusa hepatitisa B u hepatocite, imunološki napad na zaražene hepatocite izazivaju T-ubojice, koje izlučuju limfotoksine u smjeru stanica jetre.
Točni mehanizmi oštećenja hepatocita kod hepatitisa B još nisu utvrđeni. Vodeću ulogu igraju aktivirani procesi lipidne peroksidacije i lizosomskih hidrolaza. Okidač mogu biti limfotoksini oslobođeni iz efektorskih stanica pri njihovom kontaktu s hepatocitima, ali moguće je da je sam virus inicijator procesa peroksidacije. Nakon toga, patološki proces se najvjerojatnije razvija sljedećim redoslijedom.
- Interakcija faktora agresije (limfotoksini ili virus) s biološkim makromolekulama (moguće s komponentama membrana endoplazmatskog retikuluma sposobnim sudjelovati u procesima detoksikacije, analogno drugim štetnim agensima, kao što je pokazano u odnosu na ugljikov tetraklorid).
- Stvaranje slobodnih radikala, aktivacija procesa lipidne peroksidacije i povećana propusnost svih hepatocelularnih membrana (sindrom citolize).
- Kretanje biološki aktivnih tvari duž gradijenta koncentracije - gubitak enzima različitih unutarstaničnih lokalizacija, donora energije, kalija itd. Nakupljanje natrija i kalcija u stanicama, pomicanje pH prema unutarstaničnoj acidozi.
- Aktivacija i oslobađanje lizosomskih hidrolaza (RNAza, DNAza, katepsina itd.) s razgradnjom stanica jetre i oslobađanjem autoantigena.
- Stimulacija T- i B-imunološkog sustava stvaranjem specifične senzibilizacije T-limfocita na lipoproteine jetre, kao i stvaranjem antihepatičnih humoralnih autoantitijela.
U predloženoj shemi patogeneze hepatitisa B, okidački faktor su virusni antigeni, čija se intenzivna proizvodnja opaža u najranijim fazama bolesti i tijekom cijelog akutnog razdoblja, s izuzetkom malignih oblika, kod kojih proizvodnja virusnih antigena praktički prestaje u trenutku razvoja masivne nekroze jetre, što predodređuje brzo smanjenje replikacije virusa.
Također je očito da virusni antigeni aktiviraju T- i B-sustav imuniteta. Tijekom tog procesa dolazi do karakteristične preraspodjele subpopulacija T-limfocita, usmjerene na organiziranje adekvatnog imunološkog odgovora, eliminaciju zaraženih hepatocita, neutralizaciju virusnih antigena, sanogenezu i oporavak.
Kada imunokompetentne stanice stupe u interakciju s virusnim antigenima na membranama hepatocita ili tijekom reprodukcije virusa unutar hepatocita, nastaju uvjeti za aktivaciju procesa lipidne peroksidacije, koja, kao što je poznato, kontrolira propusnost svih staničnih i subcelularnih membrana.
S ove pozicije, pojava sindroma citolize, povećane propusnosti staničnih membrana, koja je toliko prirodna i vrlo karakteristična za virusni hepatitis, postaje razumljiva.
Konačni ishod sindroma citolize može biti potpuno odvajanje oksidativne fosforilacije, curenje staničnog materijala i smrt parenhima jetre.
Međutim, u velikoj većini slučajeva ti procesi ne dobivaju tako koban razvoj. Samo kod malignih oblika bolesti patološki proces teče lavinski i nepovratno, budući da dolazi do masivne infekcije, izraženog imunološkog procesa, prekomjerne aktivacije procesa peroksidacije i lizosomskih hidrodaza te pojava autoimune agresije.
Isti mehanizmi se opažaju i kod povoljnog tijeka hepatitisa B, s jedinom osobitošću da se svi ostvaruju na kvalitativno drugačijoj razini. Za razliku od slučajeva masivne nekroze jetre, kod povoljnog tijeka bolesti broj zaraženih hepatocita, a time i zona imunopatološke citolize, je manji, procesi lipidne peroksidacije nisu toliko značajno pojačani, aktivacija kiselih hidrolaza dovodi samo do ograničene autolize uz neznatno oslobađanje autoantigena, te stoga, bez masivne autoagresije, odnosno sve faze patogeneze kod povoljnog tijeka provode se u okviru očuvane strukturne organizacije parenhima jetre i ograničene su obrambenim sustavima (antioksidansi, inhibitori itd.) te stoga nemaju tako destruktivan učinak.
Uzroci simptoma intoksikacije kod virusnog hepatitisa nisu u potpunosti proučeni. Prijedlog razlikovanja takozvane primarne ili virusne intoksikacije od sekundarne (izmjenske ili metaboličke) može se smatrati pozitivnim, iako to ne otkriva intimni mehanizam nastanka općeg toksičnog sindroma. Prvo, virusi hepatitisa nemaju toksična svojstva, a drugo, koncentracija mnogih metabolita ne korelira uvijek s težinom bolesti i stupnjem izraženosti simptoma toksikoze. Također je poznato da koncentracija virusnih antigena ne korelira strogo s težinom intoksikacije. Naprotiv, s porastom težine bolesti, a time i porastom stupnja toksikoze, koncentracija HBsAg se smanjuje i najniža je kod malignih oblika u vrijeme početka duboke hepatičke kome. Istodobno, učestalost detekcije i titri specifičnih antivirusnih antitijela izravno ovise o težini bolesti.
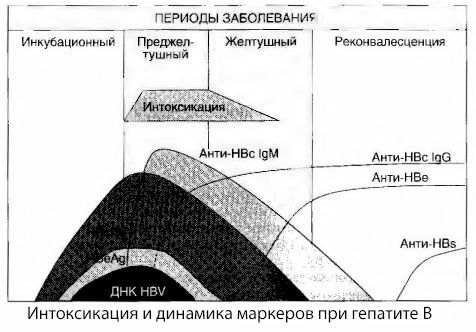
Intoksikacija se ne pojavljuje u trenutku registracije virusnih antigena, već tijekom razdoblja cirkulacije u krvi antivirusnih antitijela klase IgM na kravlji antigen i antigen E sustava. Štoviše, kod teških, a posebno malignih oblika, značajan udio pacijenata čak ima anti-HBs u krvi, što se obično nikada ne opaža kod blagih i umjerenih oblika bolesti.
Prikazani podaci omogućuju nam zaključak da sindrom toksikoze kod virusnog hepatitisa, a posebno hepatitisa B, ne nastaje kao rezultat pojave virusnih antigena u krvi, već je posljedica interakcije virusnih antigena s antivirusnim antitijelima klase IgM. Rezultat takve interakcije, kao što je poznato, je stvaranje imunoloških kompleksa i, moguće, aktivnih toksičnih tvari.
Simptomi intoksikacije nastaju u trenutku pojave imunoloških kompleksa u slobodnoj cirkulaciji, ali naknadno se takva korelacija ne opaža.
Djelomično objašnjenje za to može se pronaći u proučavanju sastava imunoloških kompleksa. Kod pacijenata s teškim oblicima, u krvi cirkuliraju pretežno kompleksi srednje veličine, a u njihovom sastavu, na vrhuncu toksičnog sindroma, prevladavaju antitijela klase, dok tijekom razdoblja pada kliničkih manifestacija i rekonvalescencije kompleksi postaju veći, a u njihovom sastavu počinju prevladavati antitijela klase IgG.
Prikazani podaci odnose se na mehanizme razvoja toksičnog sindroma u početnom razdoblju bolesti, ali kod toksikoze koja se javlja na vrhuncu kliničkih manifestacija imaju samo djelomičan značaj, a posebno kod razvoja hepatičke kome.
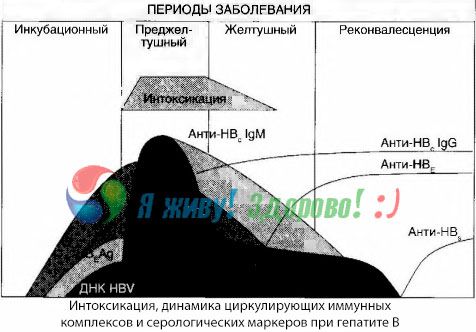
Metoda hemokultura pokazala je da se kod hepatitisa B toksini stalno nakupljaju u krvi, oslobađajući se iz oštećenog, raspadajućeg tkiva jetre. Koncentracija tih toksina proporcionalna je težini bolesti, proteinske su prirode.
Tijekom razdoblja oporavka, antitijela na ovaj toksin pojavljuju se u krvi; ali u slučaju hepatičke kome, koncentracija toksina u krvi naglo raste, a antitijela se ne otkrivaju u krvi.
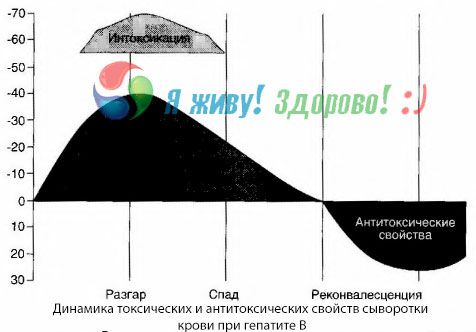
Patomorfologija hepatitisa B
Na temelju prirode morfoloških promjena razlikuju se tri oblika akutnog hepatitisa B:
- ciklički oblik,
- masivna nekroza jetre;
- kolestatski periholangiolitički hepatitis.
U cikličkom obliku hepatitisa B, distrofične, upalne i proliferativne promjene su izraženije u središtu lobula, dok su kod hepatitisa A lokalizirane duž periferije lobula, šireći se prema središtu. Ove razlike objašnjavaju se različitim putovima prodiranja virusa u parenhim jetre. Virus hepatitisa A ulazi u jetru kroz portalnu venu i širi se u središte lobula, virus hepatitisa B prodire kroz jetrenu arteriju i kapilarne grane koje ravnomjerno opskrbljuju sve lobule, sve do njihovog središta.
Stupanj oštećenja parenhima jetre u većini slučajeva odgovara težini kliničkih manifestacija bolesti. U blagim oblicima obično se opaža fokalna nekroza hepatocita, a u umjerenim i teškim oblicima - zonska nekroza (s tendencijom spajanja i stvaranja nekroze nalik mostu u teškim oblicima bolesti).
Najveće morfološke promjene u parenhimu opažaju se na vrhuncu kliničkih manifestacija, što se obično poklapa s prvim desetljećem bolesti. Tijekom 2., a posebno 3. desetljeća, regeneracijski procesi se intenziviraju. Do tog razdoblja nekrobiotičke promjene gotovo u potpunosti nestaju, a počinju prevladavati procesi stanične infiltracije s polaganom naknadnom obnovom strukture hepatocelularnih ploča. Međutim, potpuna obnova strukture i funkcije parenhima jetre događa se tek 3-6 mjeseci nakon početka bolesti i to ne kod svih pacijenata.
Generalizirana priroda infekcije kod hepatitisa B potvrđuje se detekcijom HBsAg ne samo u hepatocitima, već i u bubrezima, plućima, slezeni, gušterači, stanicama koštane srži itd.
Kolestatski (periholangiolitički) hepatitis je poseban oblik bolesti, kod kojeg se najveće morfološke promjene nalaze na strani intrahepatičnih žučnih vodova, sa slikom kolangiolitisa i periholangiolitisa. U kolestatskom obliku, kolestaza se javlja s dilatacijom žučnih kapilara sa stazom žuči u njima, s proliferacijom kolangiola i staničnim infiltratima oko njih. Stanice jetre su u ovom obliku hepatitisa neznatno zahvaćene. Klinički, bolest karakterizira dugotrajan tijek s produljenom žuticom. Pokazalo se da je uzrok tako osebujnog tijeka bolesti pretežni učinak virusa na stijenke kolangiola s neznatnim učinkom na hepatocite.

