Medicinski stručnjak članka
Nove publikacije
Uobičajena neželjena trudnoća - uzroci
Posljednji pregledao: 04.07.2025

Svi iLive sadržaji medicinski se pregledavaju ili provjeravaju kako bi se osigurala što je moguće točnija činjenica.
Imamo stroge smjernice za pronalaženje izvora i samo povezujemo s uglednim medijskim stranicama, akademskim istraživačkim institucijama i, kad god je to moguće, medicinski pregledanim studijama. Imajte na umu da su brojevi u zagradama ([1], [2], itd.) Poveznice koje se mogu kliknuti na ove studije.
Ako smatrate da je bilo koji od naših sadržaja netočan, zastario ili na neki drugi način upitan, odaberite ga i pritisnite Ctrl + Enter.
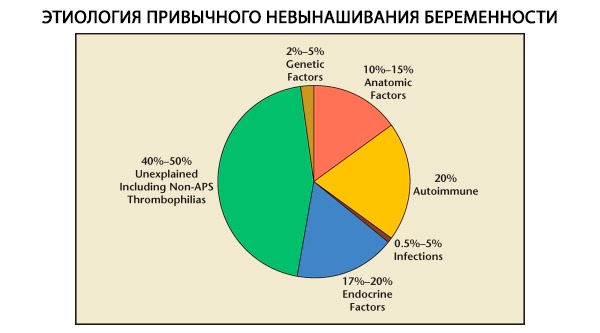
U strukturi habitualnih pobačaja razlikuju se genetski, anatomski, endokrini, imunološki i infektivni čimbenici. Kada se isključe svi navedeni uzroci, ostaje skupina pacijentica kod kojih je podrijetlo habitualnog pobačaja nejasno (idiopatski pobačaji). Prema C. Coulamu i sur. (1996.), 80% idiopatskih pobačaja temelji se na neprepoznatim imunološkim poremećajima.
Ne postoje uvjerljivi dokazi da endometrioza uzrokuje ponavljajuće spontane pobačaje ili da medicinsko ili kirurško liječenje endometrioze smanjuje učestalost ponavljajućih spontanih pobačaja.
Prema trenutnim konceptima, osim genetskih i djelomično zaraznih uzroka koji dovode do stvaranja abnormalnog embrija, provedba štetnog učinka drugih čimbenika (anatomskih, endokrinih, imunoloških) sastoji se u stvaranju nepovoljne pozadine za razvoj genetski potpunog oplođenog jajašca, što dovodi do iscrpljivanja rezervnog kapaciteta koriona i prestanka razvoja (embriogeneze). Kritična razdoblja u prvom tromjesečju trudnoće prepoznaju se kao 6-8 tjedana (smrt embrija) i 10-12 tjedana (izbacivanje oplođenog jajašca).
 [ 1 ]
[ 1 ]
Genetski uzroci uobičajenog pobačaja
Genetski čimbenici čine 3–6% uzroka habitualnih pobačaja. Kod sporadičnih prekida trudnoće u prvom tromjesečju, oko 50% pobačaja ima kromosomske abnormalnosti. Većina njih (95%) su promjene u broju kromosoma - monosomija (gubitak jednog kromosoma), trisomija (prisutnost dodatnog kromosoma), koje su rezultat pogrešaka u mejozi, kao i poliploidija (povećanje sastava kromosoma za puni haploidni set), koja nastaje kada jajnu stanicu oplode dva ili više spermija. Kod sporadičnih pobačaja najčešće se susreće trisomija - 60% svih mutacija (najčešće na kromosomu 16, kao i 13, 18, 21, 22), na drugom mjestu po učestalosti je Shereshevsky-Turnerov sindrom (kromosom 45 X0) - 20%, preostalih 15% otpada na poliploidiju (posebno triploidiju).
U slučaju promjene broja kromosoma kod pobačaja, pregled kariotipa roditelja najčešće ne otkriva nikakvu patologiju, a vjerojatnost kromosomske bolesti fetusa tijekom sljedeće trudnoće iznosi 1%. Nasuprot tome, pri pregledu pobačaja kod parova s habitualnim pobačajem, strukturne promjene kromosoma (intra- i interkromosomske) uočavaju se u 3-6% slučajeva. Pri pregledu kariotipa roditelja, uravnoteženi kromosomski preuređenji nalaze se u 7% slučajeva. Najčešće se radi o recipročnim translokacijama, kod kojih se segment jednog kromosoma nalazi na mjestu drugog segmenta nehomolognog kromosoma, kao i o mozaicizmu spolnih kromosoma, inverziji i detekciji kromosoma u obliku prstena. U slučaju prisutnosti takvih preuređenja kod jednog od supružnika, procesi sparivanja i razdvajanja kromosoma su otežani tijekom mejoze, što rezultira gubitkom (delecijom) ili udvostručenjem (duplikacijom) kromosomskih dijelova u gametama. To rezultira takozvanim neuravnoteženim kromosomskim preuređenjima, kod kojih je embrij ili nesposoban za život ili služi kao nositelj teške kromosomske patologije. Vjerojatnost rađanja djeteta s neuravnoteženim kromosomskim abnormalnostima u prisutnosti uravnoteženih kromosomskih preuređenja u kariotipu jednog od roditelja iznosi 1–15%. Razlike u podacima povezane su s prirodom preuređenja, veličinom uključenih segmenata, spolom nositelja i obiteljskom anamnezom.
Dijagnostika
Anamneza
- Nasljedne bolesti kod članova obitelji.
- Prisutnost kongenitalnih anomalija u obitelji.
- Rađanje djece s mentalnom retardacijom.
- Prisutnost neplodnosti i/ili pobačaja nepoznatog podrijetla kod bračnog para ili kod rođaka.
- Prisutnost nejasnih slučajeva perinatalne smrtnosti.
Posebne metode istraživanja
- Proučavanje kariotipa roditelja posebno je indicirano kod bračnih parova pri rođenju novorođenčeta s razvojnim manama uz anamnezu spontanog pobačaja, kao i u slučajevima uobičajenog spontanog pobačaja u ranoj trudnoći.
- Citogenetska analiza pobačaja u slučajevima mrtvorođenčeta ili neonatalne smrtnosti.
Indikacije za konzultacije s drugim specijalistima
Ako se kod roditelja otkriju promjene u kariotipu, potrebna je konzultacija s genetičarom kako bi se procijenio stupanj rizika od rađanja djeteta s patologijom ili, ako je potrebno, odlučilo o pitanju doniranja jajne stanice ili sperme.
Daljnje liječenje pacijenta
Ako bračni par ima patološki kariotip, čak i kod jednog od roditelja, preporučuje se provođenje prenatalne dijagnostike tijekom trudnoće - korionska biopsija ili amniocenteza - zbog visokog rizika od razvojnih poremećaja kod fetusa.
Anatomski uzroci habitualnog pobačaja
Anatomski uzroci habitualnog pobačaja uključuju:
- kongenitalne anomalije u razvoju maternice (potpuno udvostručenje maternice; dvorogasta, sedlasta, jednorogasta maternica; djelomična ili potpuna intrauterina pregrada);
- stečeni anatomski defekti;
- intrauterine adhezije (Ashermanov sindrom);
- submukozni fibroidi maternice;
- istmičko-cervikalna insuficijencija.
Učestalost anatomskih anomalija kod pacijentica s habitualnim spontanim pobačajem kreće se od 10 do 16%. Učestalost pojave malformacija maternice koje mogu rezultirati spontanim pobačajem (ali ne i neplodnošću) u odnosu na sve malformacije maternice je sljedeća: dvoroga maternica - 37%, sedlasta maternica - 15%, intrauterina pregrada - 22%, potpuno udvostručenje maternice - 11%, jednorogasta maternica - 4,4%.
Dijagnoza habitualnog pobačaja
Anamneza
U slučaju anatomske patologije maternice, češće se opažaju kasni prekidi trudnoće i prijevremeni porođaji, međutim, s implantacijom na intrauterinom septumu ili blizu miomatoznog čvora, mogući su i rani prekidi trudnoće.
Za istmičko-cervikalnu insuficijenciju, patognomonični znak je spontani prekid trudnoće u drugom tromjesečju ili rani prijevremeni porod, koji se događa relativno brzo i uz malo boli.
U slučaju malformacija maternice potrebno je obratiti pozornost na anamnestičke indikacije patologije mokraćnog sustava (često prateće kongenitalne anomalije maternice) i prirodu razvoja menstrualne funkcije (indikacije hematometre s funkcionalnim rudimentarnim rogom maternice).
Posebne metode ispitivanja
- Trenutno se histerosalpingografija izvodi radi postavljanja dijagnoze, što omogućuje proučavanje oblika šupljine maternice, utvrđivanje prisutnosti submukoznih fibroma, priraslica, septa i određivanje prohodnosti jajovoda. Kako bi se dijagnosticirala patologija maternice, racionalno je provoditi histerosalpingografiju u razdoblju između menstruacije i ovulacije, tj. u prvoj fazi menstrualnog ciklusa nakon prestanka krvavog iscjetka (7.-9. dan ciklusa). Za dijagnosticiranje istomsko-cervikalne insuficijencije, studija se provodi u drugoj fazi menstrualnog ciklusa (18.-20. dan) kako bi se utvrdilo stanje unutarnjeg otvora vrata maternice. Prije izvođenja histerosalpingografije potrebno je isključiti upalne bolesti zdjeličnih organa ili ih liječiti.
- Histeroskopija je posljednjih godina postala široko rasprostranjena i postala je zlatni standard za dijagnosticiranje intrauterine patologije. Međutim, zbog veće cijene u usporedbi s histerosalpingografijom, metoda se koristi kod žena s indikacijom intrauterine patologije na temelju preliminarnih ultrazvučnih podataka. Histeroskopijom se može pregledati šupljina maternice, utvrditi priroda intrauterine patologije te, ako je dostupna potrebna oprema (resektoskop), provesti minimalno invazivni kirurški tretman - uklanjanje priraslica, submukoznih miomskih čvorova i endometrijskih polipa. Prilikom uklanjanja intrauterine pregrade, prednost se daje histerosektoskopiji s laparoskopskom kontrolom, što sprječava mogućnost perforacije stijenke maternice.
- Ultrazvuk se izvodi u prvoj fazi menstrualnog ciklusa, što omogućuje pretpostavljenu dijagnozu submukoznog mioma maternice, intrauterinih priraslica, a u drugoj fazi ciklusa - identifikaciju intrauterinog septuma i bikornuatne maternice. Ova metoda je od posebne važnosti u ranoj trudnoći, kada je njezina osjetljivost u dijagnosticiranju ovih stanja 100%, a specifičnost 80%. Izvan trudnoće, dijagnoza zahtijeva dodatnu potvrdu drugim metodama.
- Strani autori ističu prednost sonohisterografije (ultrazvuk transvaginalnim senzorom s prethodnim uvođenjem 0,9%-tne otopine natrijevog klorida u šupljinu maternice) u odnosu na histerosalpingografiju, jer omogućuje diferencijalnu dijagnostiku između intrauterinog septuma i dvoroge maternice. Sonohisterografijom je moguće ne samo proučavati oblik šupljine maternice, već i odrediti konfiguraciju fundusa tijela maternice. U našoj zemlji ova metoda nije postala široko rasprostranjena.
- U nekim složenim slučajevima, magnetska rezonancija zdjeličnih organa koristi se za provjeru dijagnoze. Metoda omogućuje dobivanje vrijednih informacija u slučaju razvojnih anomalija maternice praćenih atipičnim rasporedom organa u zdjelici. Magnetska rezonancija je važna u slučaju rudimentarnog roga maternice kako bi se odlučilo je li ga preporučljivo ukloniti. Potreba za uklanjanjem rudimentarnog roga maternice javlja se u slučaju njegove povezanosti s jajovodom i jajnikom kako bi se spriječilo stvaranje i razvoj oplođene jajne stanice u njoj. Prekid trudnoće u slučaju anatomskih anomalija maternice može biti povezan s neuspješnom implantacijom oplođene jajne stanice (na intrauterinom septumu, blizu submukoznog miomskog čvora), nedovoljno razvijenom vaskularizacijom i recepcijom endometrija, bliskim prostornim odnosima u šupljini maternice (na primjer, u slučaju deformacije šupljine miomskim čvorom), često praćenim ICI-jem, te hormonskim poremećajima.
Liječenje habitualnog pobačaja
Kirurško liječenje
U prisutnosti intrauterinog septuma, submukoznih miomskih čvorova i priraslica, najučinkovitije kirurško liječenje je histeroresektoskopija. Učestalost naknadnih pobačaja u ovoj skupini žena nakon liječenja iznosi 10% u usporedbi s 90% prije operacije. Uspoređujući rezultate metroplastike izvedene laparotomijom i transcervikalnom histeroresektoskopijom, P. Heinonen (1997.) dobio je rezultate koji ukazuju na manju traumu i veću učinkovitost histeroresektoskopije; postotak trudnoća koje su rezultirale rođenjem održive djece bio je 68 odnosno 86%.
Kirurško uklanjanje intrauterinog septuma, priraslica i submukoznih miomskih čvorova eliminira pobačaj u 70–80% slučajeva. Međutim, neučinkovito je kod žena s malformacijama maternice koje su imale normalne porode s naknadnim ponavljajućim pobačajima. Vjerojatno je da u takvim slučajevima anatomski faktor nije vodeći uzrok te je potrebno tražiti druge uzroke pobačaja.
Dokazano je da je abdominalna metroplastika povezana sa značajnim rizikom od postoperativne neplodnosti i ne poboljšava prognozu sljedeće trudnoće. Stoga je bolje dati prednost histeroskopiji i laparoskopskim operacijama.
Liječenje lijekovima
Učinkovitost uvođenja spirale, visokih doza estrogenih lijekova, uvođenja Foleyjevog katetera u šupljinu maternice nakon operacija uklanjanja priraslica, intrauterinog septuma nije dokazana. Preporučuje se planiranje trudnoće najranije 3 mjeseca nakon operacije. Za poboljšanje rasta endometrija provodi se ciklička hormonska terapija tijekom 3 menstrualna ciklusa [14]. Tijekom 3 mjeseca u prvih 14 dana ciklusa preporučljivo je uzimati lijek koji sadrži 2 mg 17-beta-estradiola, u sljedećih 14 dana - 2 mg 17-beta-estradiola i 20 mg didrogesterona (10 mg didrogesterona kao dio kombiniranog lijeka plus 10 mg didrogesterona u zasebnom obliku tableta).
Daljnje liječenje pacijenta
Značajke tijeka trudnoće s dvorogom maternicom ili udvostručenjem maternice (kada postoje 2 maternične šupljine):
- u ranoj trudnoći krvarenje se često javlja iz "praznog" roga ili šupljine maternice zbog izražene decidualne reakcije; taktika u ovom slučaju treba biti konzervativna i sastojati se od upotrebe antispazmodičkih i hemostatskih sredstava;
- prijetnja prekida trudnoće u različitim fazama;
- razvoj isthmičko-cervikalne insuficijencije;
- intrauterini zastoj u rastu zbog placentalne insuficijencije.
U ranoj trudnoći, u slučaju krvarenja, preporučljivo je mirovanje u krevetu i polu-posteljno mirovanje, primjena hemostatičkih, antispazmodičnih i sedativnih lijekova te terapija gestagenima (didrogesteron u dnevnoj dozi od 20 do 40 mg) do 16–18 tjedana trudnoće.
Endokrini uzroci habitualnog pobačaja
Prema raznim autorima, endokrini uzroci pobačaja čine 8 do 20%. Najznačajniji od njih su nedostatak lutealne faze (LPD), hipersekrecija LH, disfunkcija štitnjače i dijabetes melitus.
Teška bolest štitnjače ili dijabetes melitus mogu dovesti do ponovljenih pobačaja. Međutim, kod kompenziranog dijabetesa melitusa rizik od uobičajenih pobačaja ne razlikuje se od rizika u općoj populaciji.
Istodobno, visoka incidencija hipotireoze u populaciji zahtijeva probir s mjerenjem razine TSH. Kod pacijentica s habitualnim spontanim pobačajem, insuficijencija lutealne faze opaža se u 20–60% slučajeva, a ultrazvučni znakovi policističnih jajnika u 44–56%. Prema literaturi, utjecaj pojedinačnih hormonalnih poremećaja na formiranje simptomskog kompleksa habitualnog spontanog pobačaja ostaje kontroverzan. Studije M. Ogasaware i sur. (1997.) nisu otkrile pouzdane razlike u učestalosti prekida trudnoće s i bez LPI kod pacijentica s dva ili više prethodnih spontanih pobačaja u anamnezi, isključujući autoimune, anatomske i infektivne uzroke.
Nedovoljna funkcija žutog tijela može biti posljedica niza nepovoljnih čimbenika:
- poremećaji u lučenju FSH i LH u prvoj fazi menstrualnog ciklusa;
- rani ili, obrnuto, prekasni vrhunac oslobađanja LH;
- hipoestrogenizam kao posljedica neadekvatne folikulogeneze. Sva ova stanja ne podliježu korekciji nadomjesnom terapijom gestagenim lijekovima u postovulatornom razdoblju. Prospektivne studije koje su proveli L. Regan i suradnici pokazale su značajan porast učestalosti pobačaja kod pacijentica s hipersekrecijom LH 8. dana menstrualnog ciklusa u usporedbi sa ženama s normalnom razinom LH u krvi (65% odnosno 12% pobačaja). Štetni učinak preranog porasta LH povezan je s preranim nastavkom druge mejotičke diobe i ovulacijom nezrele jajne stanice, kao i s indukcijom proizvodnje androgena teka stanicama uz poremećenu recepciju endometrija pod utjecajem insuficijencije gestagena. Međutim, prethodno smanjenje preovulatorne razine LH agonistima hormona koji oslobađa gonadotropin bez dodatnih mjera usmjerenih na produljenje naknadne trudnoće ne osigurava očekivano smanjenje učestalosti pobačaja.
Zlatni standard za dijagnosticiranje NLF-a je histološki pregled materijala dobivenog biopsijom endometrija u drugoj fazi ciklusa tijekom 2 menstrualna ciklusa.
Dijagnoza drugih uzroka ovulacijske disfunkcije, poput hiperprolaktinemije, hipotireoze, funkcionalnog viška androgena (jajnika ili nadbubrežnih žlijezda), mora biti popraćena propisivanjem odgovarajućeg liječenja.
Dijagnostika
Anamneza i fizikalni pregled
- Anamneza. Čimbenici koje treba uzeti u obzir: kasna menarha, neredovit menstrualni ciklus (oligomenoreja, amenoreja, naglo debljanje, gubitak težine, neplodnost, uobičajeni rani pobačaji).
- Pregled: tip tijela, visina, tjelesna težina, hirzutizam, izraženost sekundarnih spolnih karakteristika, prisutnost strija, pregled mliječnih žlijezda na galaktoreju.
- Funkcionalni dijagnostički testovi: mjerenje rektalne temperature tijekom 3 menstrualna ciklusa.
Posebne metode istraživanja
- Hormonska studija:
- u 1. fazi menstrualnog ciklusa (7-8. dan) – određivanje sadržaja FSH, LH, prolaktina, TSH, testosterona, 17-hidroksiprogesterona (17-OP), DHEAS-a;
- u 2. fazi menstrualnog ciklusa (21–22 dana) – određivanje sadržaja progesterona (normativni pokazatelji razine progesterona su vrlo varijabilni, metoda se ne može koristiti bez uzimanja u obzir drugih čimbenika).
- Ultrazvuk:
- u 1. fazi menstrualnog ciklusa (5.–7. dan) – dijagnoza patologije endometrija, policističnih jajnika;
- u 2. fazi menstrualnog ciklusa (20–21 dan) – mjerenje debljine endometrija (normalno 10–11 mm, korelira s sadržajem progesterona).
- Biopsija endometrija za provjeru NLF-a izvodi se 2 dana prije očekivane menstruacije (26. dana kod ciklusa od 28 dana). Ova se metoda koristi u slučajevima kada je dijagnoza nejasna. Za proučavanje promjena u endometriju u tzv. razdoblju "implantacijskog prozora", biopsija se izvodi 6. dana nakon ovulacije.
Liječenje
Prilikom dijagnosticiranja NLF-a (prema rektalnim temperaturnim grafikonima, trajanje 2. faze je manje od 11 dana, opaža se postupni porast temperature, nedovoljna sekretorna transformacija endometrija prema podacima biopsije endometrija, niske razine progesterona u krvnom serumu), potrebno je utvrditi uzrok takvih poremećaja.
Ako je NLF popraćen hiperprolaktinemijom, izvodi se magnetska rezonancija mozga. Alternativna metoda je rendgenska snimka lubanje (regija sella turcica).
Prva faza kod hiperprolaktinemije je isključivanje adenoma hipofize, što zahtijeva kirurško liječenje. U nedostatku značajnih promjena, hiperprolaktinemija se smatra funkcionalnom, a liječenje bromokriptinom propisuje se za normalizaciju razine prolaktina. Početna doza bromokriptina je 1,25 mg/dan tijekom 2 tjedna, nakon praćenja razine prolaktina, ako se pokazatelji ne normaliziraju, doza se povećava na 2,5 mg/dan. Uz značajan porast razine prolaktina, početna doza je 2,5 mg/dan. Ako dođe do trudnoće, bromokriptin treba prekinuti.
Ako se otkrije hipotireoza, priroda patologije štitnjače utvrđuje se zajedno s endokrinologom. U svakom slučaju, indicirana je dnevna terapija natrijevim levotiroksinom, doza se odabire individualno dok se razina TSH ne normalizira. Ako dođe do trudnoće, liječenje natrijevim levotiroksinom treba nastaviti. Pitanje o preporučljivosti povećanja doze u prvom tromjesečju trudnoće odlučuje se zajedno s endokrinologom nakon dobivanja rezultata hormonskog pregleda (razina TSH, slobodni tiroksin).
Korekcija NLF-a provodi se na jedan od dva načina. Prvi način je stimulacija ovulacije, drugi način je nadomjesna terapija pripravcima progesterona.
Prva mogućnost liječenja je stimulacija ovulacije klomifen citratom. Ova metoda liječenja temelji se na činjenici da se većina poremećaja lutealne faze javlja u folikularnoj fazi ciklusa. Stalno snižene razine progesterona u 2. fazi posljedica su poremećene folikulogeneze u 1. fazi ciklusa. Ovaj poremećaj će se s većim uspjehom ispraviti niskim dozama klomifen citrata u ranoj folikularnoj fazi nego propisivanjem progesterona u 2. fazi ciklusa.
U 1. ciklusu, doza klomifen citrata je 50 mg/dan od 5. do 9. dana menstrualnog ciklusa. Učinkovitost se prati pomoću rektalnih temperaturnih grafikona, mjerenja razine progesterona u 2. fazi ciklusa ili dinamičkog ultrazvuka. Ako nema dovoljnog učinka u 2. ciklusu stimulacije ovulacije, dozu klomifen citrata treba povećati na 100 mg/dan od 5. do 9. dana ciklusa. Maksimalna moguća doza u 3. ciklusu stimulacije ovulacije je 150 mg/dan. Takvo povećanje doze moguće je samo ako se lijek dobro podnosi (nema intenzivne boli u donjem dijelu trbuha i donjem dijelu leđa te nema drugih znakova hiperstimulacije jajnika).
Druga mogućnost liječenja: nadomjesna terapija progesteronskim pripravcima, koji potiču potpunu sekretornu transformaciju endometrija, što daje potreban učinak kod pacijentica s habitualnim pobačajem s očuvanom ovulacijom. Osim toga, posljednjih je godina utvrđeno da primjena progesteronskih pripravaka ima ne samo hormonski, već i imunomodulatorni učinak, suzbijajući reakcije odbacivanja imunokompetentnih stanica u endometriju. Posebno je sličan učinak opisan za dihidrogesteron u dozi od 20 mg/dan. U svrhu nadomjesne terapije, didrogesteron se koristi u dozi od 20 mg/dan oralno ili mikronizirani progesteron vaginalno u dozi od 200 mg/dan. Liječenje se provodi 2. dana nakon ovulacije (dan nakon porasta rektalne temperature) i nastavlja se 10 dana. Ako dođe do trudnoće, liječenje progesteronskim pripravcima treba nastaviti.
Suvremena istraživanja nisu potvrdila učinkovitost humanog korionskog gonadotropina u liječenju ponavljajućih pobačaja.
Kod hiperandrogenizma (jajničke ili nadbubrežne geneze) kod pacijentica s habitualnim pobačajem indicirano je liječenje lijekovima zbog utjecaja androgena na potpunost ovulacije i stanje endometrija. U slučaju kršenja biosinteze nadbubrežnih androgena, moguć je njihov virilizirajući učinak na ženski fetus, stoga se steroidna terapija provodi u interesu fetusa.
Hiperandrogenizam ovarijalnog porijekla (policistični jajnici)
Anamneza, fizikalni pregled i rezultati specijalističkog pregleda
- Anamneza: kasna menarha, poremećaji menstrualnog ciklusa poput oligomenoreje (obično primarna, rjeđe sekundarna). Trudnoće su rijetke, obično spontano prekinute u prvom tromjesečju, s dugim razdobljima neplodnosti između trudnoća.
- Pregled: hirzutizam, akne, strije, visoki indeks tjelesne mase (opcionalno).
- Rektalni temperaturni grafikoni: anovulacijski ciklusi se izmjenjuju s ciklusima s ovulacijom i NLF-om.
- Hormonski pregled: visoke razine testosterona, razine FSH i LH mogu biti povišene, omjer LH/FSH je veći od 3. Ultrazvuk: policistični jajnici.
Liječenje
Liječenje bez lijekova
Mršavljenje - dijetoterapija, tjelesna aktivnost.
Liječenje lijekovima
- Orlistat u dozi od 120 mg uz svaki glavni obrok. Trajanje tečaja određuje se uzimajući u obzir učinak i podnošljivost.
- Preliminarno smanjenje testosterona pripravcima koji sadrže ciproteron acetat (2 mg) i EE (35 mcg) tijekom 3 menstrualna ciklusa.
- Prekid kontracepcije, hormonska podrška drugoj fazi ciklusa (terapija gestagenima) - didrogesteron u dozi od 20 mg/dan od 16. do 25. dana menstrualnog ciklusa. Ako nema spontane ovulacije, prijeći na sljedeću fazu.
- Stimulacija ovulacije klomifen citratom u početnoj dozi od 50 mg/dan od 5. do 9. dana menstrualnog ciklusa uz istovremenu terapiju gestagenima (didrogesteron u dozi od 20 mg/dan od 16. do 25. dana ciklusa) i deksametazonom (0,5 mg).
- U nedostatku trudnoće, doza klomifen citrata se povećava na 100–150 mg/dan uz primjenu gestagena u drugoj fazi ciklusa i deksametazona (0,5 mg). Utvrđeno je da, iako deksametazon smanjuje samo razinu nadbubrežnih androgena, ovulacija i začeće se značajno češće događaju uz liječenje klomifen citratom i deksametazonom nego uz primjenu samog klomifen citrata [12].
- Provode se tri ciklusa stimulacije ovulacije, nakon čega se preporučuje prekid od tri menstrualna ciklusa s gestagenom potporom i odluka o kirurškom liječenju laparoskopskim pristupom (klinasta resekcija jajnika, laserska vaporizacija).
Daljnje liječenje pacijenta
Vođenje trudnoće treba biti popraćeno gestagenom potporom do 16. tjedna trudnoće (didrogesteron u dozi od 20 mg/dan ili mikronizirani progesteron u dozi od 200 mg/dan), deksametazon se propisuje samo u prvom tromjesečju trudnoće. Praćenje je obavezno radi pravovremene dijagnoze isthmičko-cervikalne insuficijencije i, ako je potrebno, njezine kirurške korekcije.
Adrenalni hiperandrogenizam (pubertalni i postpubertalni adrenogenitalni sindrom)
Adrenogenitalni sindrom (AGS) je nasljedna bolest povezana s poremećajem sinteze hormona kore nadbubrežne žlijezde zbog oštećenja gena odgovornih za sintezu niza enzimskih sustava. Bolest se nasljeđuje autosomno recesivnim putem prijenosom mutiranih gena s oba roditelja, koji su zdravi nositelji.
U 90% slučajeva, adrenogenitalni sindrom uzrokovan je mutacijama u genu CYP21B, što dovodi do poremećaja u sintezi 21-hidroksilaze.
Anamneza, fizikalni pregled i rezultati specijalističkog pregleda
- Anamneza: kasna menarha, blago produženi menstrualni ciklus, moguća oligomenoreja, spontani pobačaji u prvom tromjesečju, moguća neplodnost.
- Pregled: akne, hirzutizam, androidni tip tijela (široka ramena, uska zdjelica), hipertrofija klitorisa.
- Rektalni temperaturni grafikoni: anovulacijski ciklusi se izmjenjuju s ciklusima s ovulacijom i NLF-om.
- Hormonski test: visoke razine 17-OP, DHEAS.
- Ultrazvuk: jajnici su nepromijenjeni.
Patognomonični znak izvan trudnoće je povećanje koncentracije 17-OP u krvnoj plazmi.
Trenutno se za dijagnosticiranje latentnog, neklasičnog oblika adrenalnog hiperandrogenizma koristi test s ACTH-om. Za ovaj test koristi se Synacthen - sintetski polipeptid koji ima svojstva endogenog ACTH-a, tj. stimulira početne faze sinteze steroidnih hormona iz kolesterola u nadbubrežnim žlijezdama.
Synacthen test (analog ACTH-a): 1 ml (0,5 mg) synacthena se ubrizgava potkožno u rame, početni sadržaj 17-OP-a i kortizola se prvo određuje u jutarnjem uzorku krvne plazme nakon 9 sati. Kontrolni uzorak krvi se uzima 9 sati nakon injekcije kako bi se odredila razina 17-OP-a i kortizola. Indeks određivanja (D) se zatim izračunava pomoću formule:
D = 0,052 × 17-OP + 0,005 × kortizol/17-OP - 0,018 × kortizol/17-OP
Ako je D koeficijent manji ili jednak 0,069, to ukazuje na odsutnost adrenalnog hiperandrogenizma. Ako je D koeficijent veći od 0,069, treba uzeti u obzir da je hiperandrogenizam uzrokovan disfunkcijom nadbubrežnih žlijezda.
Liječenje lijekovima
Glavni oslonac liječenja hiperandrogenizma uzrokovanog nedostatkom 21-hidroksilaze su glukokortikoidi, koji se koriste za suzbijanje prekomjerne sekrecije androgena.
Daljnje liječenje pacijenta
Zbog virilizirajućeg učinka majčinih androgena na fetus, s utvrđenom dijagnozom adrenalnog hiperandrogenizma, liječenje deksametazonom u početnoj dozi od 0,25 mg propisuje se prije trudnoće i nastavlja se u individualno odabranoj dozi (od 0,5 do 1 mg) tijekom cijele trudnoće. Kod žene s habitualnim pobačajem koja pati od adrenalnog hiperandrogenizma, nije prikladno prekinuti liječenje, budući da učestalost pobačaja u odsutnosti liječenja doseže 14%, a s nastavkom - 9%.
S obzirom na činjenicu da pacijentice s adrenogenitalnim sindromom mogu prenijeti ovaj gen na fetus, potrebno je provesti prenatalnu dijagnostiku: u 17.-18. tjednu trudnoće propisuje se krvni test kako bi se odredio sadržaj 17-OP-a u majci. Ako je razina hormona u krvi povišena, određuje se njegova koncentracija u amnionskoj tekućini. Ako je sadržaj 17-OP-a u amnionskoj tekućini povišen, dijagnosticira se adrenogenitalni sindrom u fetusa. Nažalost, nemoguće je odrediti težinu adrenogenitalnog sindroma (blagi ili teški oblik s gubitkom soli) prema razini 17-OP-a u amnionskoj tekućini. Pitanje održavanja trudnoće u ovoj situaciji odlučuju roditelji.
Ako je otac djeteta nositelj gena adrenogenitalnog sindroma i u obitelji su zabilježeni slučajevi djece rođene s ovim sindromom, tada pacijent, čak i bez adrenalnog hiperandrogenizma, u interesu fetusa (radi sprječavanja virilizacije ženskog fetusa) prima deksametazon u dozi od 20 mcg/kg tjelesne težine, maksimalno 1,5 mg/dan u 2-3 doze nakon obroka. U 17-18 tjednu, nakon što se odluči o spolu fetusa i ekspresiji gena adrenogenitalnog sindroma (na temelju rezultata amniocenteze), liječenje se nastavlja do kraja trudnoće ako je fetus djevojčica s adrenogenitalnim sindromom. Ako je fetus dječak ili djevojčica koja nije nositelj gena adrenogenitalnog sindroma, deksametazon se može prekinuti.
Ako žena s habitualnim spontanim pobačajem pati od adrenalnog hiperandrogenizma, tada se liječenje deksametazonom provodi tijekom cijele trudnoće i prekida se tek nakon poroda. Trećeg dana nakon poroda doza deksametazona se postupno smanjuje (za 0,125 mg svaka 3 dana) do potpunog prekida u postporođajnom razdoblju.
Hiperandrogenizam miješane geneze (jajnika i nadbubrežne žlijezde)
Anamneza, fizikalni pregled i rezultati specijalističkog pregleda
- Anamneza: kasna menarha, poremećaji menstrualnog ciklusa poput oligomenoreje (obično primarne, rjeđe sekundarne), amenoreje, moguće ozljede, potresi mozga. Trudnoće su rijetke, obično spontano prekinute u prvom tromjesečju, duga razdoblja neplodnosti između trudnoća.
- Fizikalni pregled: hirzutizam, akne, strije, acanthosis nigricans, visoki indeks tjelesne mase, hipertenzija.
- Rektalni temperaturni grafikoni: anovulacijski ciklusi se izmjenjuju s ciklusima s ovulacijom i NLF-om.
- Hormonski pregled: visoke razine testosterona, mogu biti povišene razine FSH i LH, omjer LH/FSH veći od 3, visoke razine DHEAS-a, 17-OP-a, može biti prisutna hiperprolaktinemija.
- Ultrazvuk: policistični jajnici.
- Elektroencefalografija: promjene u bioelektričnoj aktivnosti mozga.
- Hiperinzulinemija, poremećaj metabolizma lipida (visok kolesterol, lipoproteini niske gustoće i lipoproteini vrlo niske gustoće), smanjena tolerancija glukoze ili povišene razine glukoze u krvi.
Liječenje
Liječenje bez lijekova
Gubitak težine (niskokalorična dijeta, tjelesna aktivnost).
Liječenje lijekovima
Prva faza - u prisutnosti inzulinske rezistencije, preporučuje se propisivanje metformina u dnevnoj dozi od 1000-1500 mg kako bi se povećala osjetljivost na inzulin.
Druga faza - u slučaju teških poremećaja menstrualnog ciklusa i visoke razine testosterona, preporučuje se propisivanje lijekova s antiandrogenim učinkom koji sadrže ciproteron acetat (2 mg) i etinil estradiol (35 mcg) tijekom 3 mjeseca.
Treća faza je stimulacija ovulacije nakon čega slijedi gestagena potpora (shema je opisana gore) i uzimanje deksametazona u dnevnoj dozi od 0,25–0,5 mg.
U slučaju hiperprolaktinemije i hipotireoze, potrebno je provesti odgovarajuću korekciju lijeka u ciklusima stimulacije ovulacije. Ako dođe do trudnoće, treba prekinuti primjenu bromokriptina i nastaviti s levotiroksinom.
Ako je stimulacija ovulacije neučinkovita, treba odlučiti o pitanju propisivanja izravnih induktora ovulacije, preporučljivosti kirurškog liječenja policističnih jajnika ili oplodnje in vitro.
Daljnje liječenje pacijenta
Kod pacijentica s metaboličkim sindromom trudnoća je često komplicirana arterijskom hipertenzijom, nefropatijom, hiperkoagulacijom, u vezi s čime je potrebno pratiti krvni tlak, hemostaziograme od ranih faza trudnoće i korigirati nastale poremećaje (ako je potrebno) antihipertenzivnim lijekovima, antitrombocitnim sredstvima i antikoagulansima. Gestageni lijekovi propisuju se do 16 tjedana trudnoće - didrogesteron u dozi od 20 mg/dan ili mikronizirani progesteron u dozi od 200 mg/dan u 2 doze.
Sve žene s hiperandrogenizmom predstavljaju rizičnu skupinu za razvoj istomsko-cervikalne insuficijencije. Praćenje stanja vrata maternice treba provoditi od 16. tjedna trudnoće, ako je potrebno - kirurška korekcija istomsko-cervikalne insuficijencije.
Imunološki uzroci habitualnog pobačaja
Trenutno je poznato da je oko 80% svih prethodno neobjašnjivih slučajeva ponovljenog gubitka trudnoće (nakon isključivanja genetskih, anatomskih i hormonalnih uzroka) povezano s imunološkim poremećajima. Razlikuju se autoimuni i aloimuni poremećaji koji dovode do habitualnog pobačaja.
U autoimunim procesima, vlastita tkiva imunološkog sustava postaju objekt agresije, tj. imunološki odgovor usmjeren je protiv vlastitih antigena. U toj situaciji fetus sekundarno pati kao posljedica oštećenja tkiva majke.
Kod aloimunih poremećaja, imunološki odgovor žene usmjeren je protiv embrionalnih/fetalnih antigena primljenih od oca, a koji su potencijalno strani majčinom tijelu.
Autoimuni poremećaji koji se najčešće javljaju kod pacijentica s habitualnim spontanim pobačajem uključuju prisutnost antifosfolipidnih, antitireoidnih i antinuklearnih autoantitijela u serumu. Tako je utvrđeno da 31% žena s habitualnim spontanim pobačajem izvan trudnoće ima autoantitijela na tireoglobulin i tireoidnu peroksidazu (tireoidna mikrosomalna [tireoidna peroksidaza] autoantitijela); u tim slučajevima rizik od spontanog pobačaja u prvom tromjesečju trudnoće raste na 20%. Kod habitualnog spontanog pobačaja, prisutnost antinuklearnih i antitireoidnih antitijela ukazuje na potrebu za daljnjim pregledom kako bi se identificirao autoimuni proces i potvrdila dijagnoza.
Antifosfolipidni sindrom (APS) ostaje općeprihvaćeno autoimuno stanje koje dovodi do smrti embrija/fetusa.
Aloimuni poremećaji
Trenutno, aloimuni procesi koji dovode do odbacivanja fetusa uključuju prisutnost povećanog (više od 3) broja zajedničkih antigena glavnog kompleksa histokompatibilnosti kod supružnika (često se opaža u srodnim brakovima); niske razine blokirajućih faktora u serumu majke; povećane razine prirodnih stanica ubojica (NK stanice CD56, CD16) u endometriju i perifernoj krvi majke i izvan i tijekom trudnoće; visoke razine koncentracije niza citokina u endometriju i krvnom serumu, posebno γ-interferona, faktora tumorske nekroze a, interleukina-1 i 2.
Trenutno se proučavaju aloimuni čimbenici koji dovode do ranih gubitaka trudnoće i načini ispravljanja gore navedenih stanja. Ne postoji konsenzus o metodama terapije. Prema nekim istraživačima, aktivna imunizacija donorskim limfocitima ne daje značajan učinak, dok drugi autori opisuju značajan pozitivan učinak kod takve imunizacije i liječenja imunoglobulinima.
Trenutno je progesteron jedan od imunomodulatornih agensa u ranoj trudnoći. Studije su posebno dokazale ulogu didrogesterona u dnevnoj dozi od 20 mg kod žena s habitualnim pobačajem u prvom tromjesečju trudnoće s povećanom razinom CD56 stanica u endometriju.
 [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
[ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
Genetski određene trombofilije
Sljedeći oblici genetski određenih trombofilija smatraju se trombofilnim stanjima tijekom trudnoće koja dovode do habitualnog pobačaja.
- Nedostatak antitrombina III.
- Mutacija faktora V (Leidenska mutacija).
- Nedostatak proteina C.
- Nedostatak proteina S.
- Mutacija gena za protrombin G20210A.
- Hiperhomocisteinemija.
Pregled za utvrđivanje rijetkih uzroka trombofilije potreban je u slučajevima kada su postojali:
- obiteljska anamneza - tromboembolija prije 40. godine života kod rođaka;
- pouzdane epizode venske i/ili arterijske tromboze prije 40. godine života;
- ponavljajuća tromboza kod pacijenta i neposrednih rođaka;
- tromboembolijske komplikacije tijekom trudnoće i nakon poroda pri korištenju hormonske kontracepcije;
- ponovljeni gubici trudnoće, mrtvorođenčad, intrauterini zastoj u rastu, abrupcija posteljice;
- preeklampsija s ranim početkom, HELLP sindrom.
Zarazni uzroci habitualnog pobačaja
Uloga infektivnog faktora kao uzroka habitualnog pobačaja trenutno je predmet širokih rasprava. Poznato je da primarna infekcija u ranoj fazi trudnoće može uzrokovati oštećenje embrija koje je nespojivo sa životom, što dovodi do sporadičnog spontanog pobačaja. Međutim, vjerojatnost reaktivacije infekcije istovremeno s ishodom ponovljenih gubitaka trudnoće je zanemariva. Osim toga, mikroorganizmi koji izazivaju habitualni pobačaj trenutno nisu pronađeni. Studije posljednjih godina pokazale su da većina žena s habitualnim pobačajem i kroničnim endometritisom ima prevalenciju 2-3 ili više vrsta obligatornih anaerobnih mikroorganizama i virusa u endometriju.
Prema VM Sidelnikovoj i sur., kod žena koje pate od habitualnog spontanog pobačaja, dijagnoza kroničnog endometritisa izvan trudnoće histološki je potvrđena u 73,1% slučajeva, a u 86,7% slučajeva uočena je perzistencija oportunističkih mikroorganizama u endometriju, što svakako može biti uzrok aktivacije imunopatoloških procesa. Mješovita perzistentna virusna infekcija (herpes simplex virus, Coxsackie A, Coxsackie B, enterovirusi 68–71, citomegalovirus) se kod pacijentica s habitualnim spontanim pobačajem nalazi značajno češće nego kod žena s normalnom opstetričkom anamnezom. K. Kohut i sur. (1997.) pokazali su da je postotak upalnih promjena u endometriju i decidualnom tkivu kod pacijentica s primarnim ponavljajućim spontanim pobačajem značajno veći nego kod žena nakon spontanog pobačaja s anamnezom barem jednog terminskog poroda.
Bakterijska i virusna kolonizacija endometrija obično je rezultat nemogućnosti imunološkog sustava i nespecifičnih zaštitnih snaga tijela (sustav komplementa, fagocitoza) da potpuno eliminiraju infektivni agens, a istovremeno je njegovo širenje ograničeno aktivacijom T-limfocita (T-pomagača, prirodnih ubojica) i makrofaga. U svim navedenim slučajevima dolazi do perzistencije mikroorganizama, koju karakterizira privlačenje mononuklearnih fagocita, prirodnih ubojica, T-pomagača, koji sintetiziraju različite citokine, na mjesto kronične upale. Očito, takvo stanje endometrija sprječava stvaranje lokalne imunosupresije u preimplantacijskom razdoblju, koja je potrebna za stvaranje zaštitne barijere i sprječavanje odbacivanja polustranog fetusa.
U tom smislu, prije trudnoće, ženama s uobičajenim spontanim pobačajem treba dijagnosticirati kronični endometritis. Kako bi se potvrdila ili isključila ova dijagnoza, provodi se biopsija endometrija 7.-8. dana menstrualnog ciklusa s histološkim pregledom, PCR-om i bakteriološkim pregledom materijala iz šupljine maternice. Prilikom provjere dijagnoze, kronični endometritis se liječi prema standardima za liječenje upalnih bolesti zdjeličnih organa.

