Medicinski stručnjak članka
Nove publikacije
Lijekovi
Lijekovi koji sprječavaju trombozu i poboljšavaju reološke karakteristike krvi
Posljednji pregledao: 07.07.2025

Svi iLive sadržaji medicinski se pregledavaju ili provjeravaju kako bi se osigurala što je moguće točnija činjenica.
Imamo stroge smjernice za pronalaženje izvora i samo povezujemo s uglednim medijskim stranicama, akademskim istraživačkim institucijama i, kad god je to moguće, medicinski pregledanim studijama. Imajte na umu da su brojevi u zagradama ([1], [2], itd.) Poveznice koje se mogu kliknuti na ove studije.
Ako smatrate da je bilo koji od naših sadržaja netočan, zastario ili na neki drugi način upitan, odaberite ga i pritisnite Ctrl + Enter.
U sprječavanju stvaranja višestrukih mikrotromba tijekom šoka i njihovog uništavanja mogu se koristiti različiti farmakološki pristupi koji koriste lijekove koji sprječavaju stvaranje tromba i poboljšavaju reologiju krvi:
- uklanjanje sistemskih hemodinamskih i mikrocirkulacijskih poremećaja korištenjem vazoaktivnih i inotropnih sredstava;
- mjere za poboljšanje reologije krvi korištenjem racionalne infuzijske terapije i lijekova koji vraćaju elastičnost membrana eritrocita (trental ili pentoksifilin);
- sprječavanje agregacije trombocita i stvaranje početnih „bijelih“ tromba u malim arterijskim žilama s naknadnim pokretanjem kaskade koagulacije;
- inhibicija stvaranja tromba nakon aktivacije sistemske kaskade koagulacije;
- aktivacija fibrinolize s ciljem otapanja novonastalih krvnih ugrušaka (fibrinolizin, streptokinaza, streptodekaza, urokinaza itd.) ili, naprotiv, inhibicija fibrinolize kada je generalizirana kod nekih pacijenata s traumatskim šokom i sepsom (aminokaproinska kiselina, amben, kontrikal itd.).
Većina navedenih pristupa su tradicionalni, dobro razvijeni u praksi liječenja šoka, imaju vlastite hemoreološke indikacije i navedeni su u odgovarajućim poglavljima. Stoga je u ovom odjeljku preporučljivo zadržati se na razmatranju općeg pristupa sprječavanju stvaranja tromba u šoku korištenjem farmakoloških sredstava koja utječu na profazu zgrušavanja krvi. Upravo ta razina sprječavanja komplikacija zgrušavanja - pojava, stvaranje i rast "bijelih arterijskih tromba" - privlači najveću pozornost istraživača.
Različiti tipovi šoka karakteriziraju različiti i često višesmjerni poremećaji koagulacije krvi s pogoršanjem njezine reologije. Najkarakterističniji za septički, endotoksinski, opeklinski, traumatski i hemoragijski tip šoka je stvaranje višestrukih mikrotromba u najmanjim žilama, uzrokovano poremećajima sistemske hemodinamike, vazospazmom i poremećajima mikrocirkulacije, zgušnjavanjem krvi, muljem, smanjenom elastičnošću membrana eritrocita, kao i brojnim općim i lokalnim čimbenicima (autokoidi) koji pokreću lokalne promjene u koagulacijskoj hemostazi i uključivanjem profaze koagulacije krvi.
U shematskom (skraćenom) obliku, početna faza hemokoagulacije i mehanizam lokalne homeostaze hemokoagulacije prikazani su na sljedeći način.
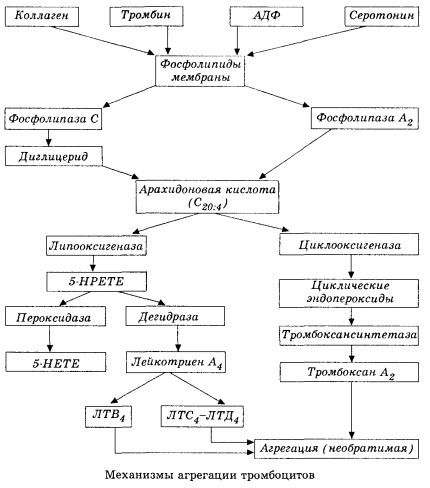
Počinje aktivacijom membranske fosfolipaze A2 kao rezultat utjecaja kombinacije štetnih čimbenika (izravno oštećenje membrane, hipoksija, lipidna peroksidacija, utjecaj endogenih kemijskih čimbenika itd.). Kao rezultat razgradnje membranskih fosfolipida oslobađaju se neesterificirane masne kiseline dugog lanca, od kojih je arahidonska kiselina najvažnija kao početni supstrat. Njena transformacija (kaskada arahidonske kiseline) odvija se putem lipoksigenaznog (sinteza leukotriena) i ciklooksigenaznog (sinteza prostaglandina, tromboksana, prostaciklina) puta.
Nastali leukotrieni (B4, C4, E4, D4 itd.) - tvari s izuzetno visokom biološkom aktivnošću, koje uključuju sporo reagirajuću tvar anafilaksije - imaju veliku važnost u pokretanju lokalnih vaskularnih, upalnih i imunoloških reakcija, uključujući autoimune procese. Leukotrieni uzrokuju poremećaje mikrocirkulacije, povećano zgrušavanje krvi, oslobađanje autolitičkih lizosomalnih enzima i oslobađanje u krv faktora koji inhibira kontraktilnost miokarda i bronhijalni spazam.
Zbog svoje sposobnosti izazivanja kontrakcije glatkih mišića, leukotrieni značajno utječu na sistemsku hemodinamiku, koronarne žile i miokard, ispoljavajući snažan koronarni konstriktorni i negativni inotropni učinak, što je popraćeno smanjenjem srčanog minutnog volumena i igra važnu ulogu u razvoju hipotenzije.
Smanjeni srčani minutni volumen i hipotenzivni odgovor na leukotriene povezani su sa slabljenjem srčanog mišića i ograničenjem venskog povratka u srce. Od značajne važnosti u ograničavanju venskog povratka je sposobnost leukotriena da povećaju propusnost vaskularne stijenke i uzrokuju ekstravazaciju plazme. Leukotrieni se smatraju važnima u patogenezi infarkta miokarda.
U anafilaktičkom i septičkom (endotoksičnom) šoku njihova uloga očito se još više povećava, što dokazuje sposobnost leukotriena da se u značajnim količinama akumuliraju u plazmi tijekom alergijskih reakcija i da uzrokuju promjene u sistemskom protoku krvi karakteristične za anafilaktički šok, kao i zaštitni učinci blokatora leukotrienskih receptora i inhibitora lipoksigenaze. Razvoj selektivnih blokatora leukotrienskih receptora provodi se prilično intenzivno i predstavlja obećavajući smjer znanosti. U tom području već je postignut određeni uspjeh, a učinkovitost takvih blokatora kod ishemije miokarda, endotoksina i hemoragijskog šoka eksperimentalno je potvrđena. Međutim, vjerojatno će proći još nekoliko godina prije nego što se ovaj smjer klinički primijeni.
Ako se u venskim žilama trombi stvaraju uz jednaku participaciju trombocita i faktora koagulacije plazme, onda su u arterijama trombociti glavni inicijatori procesa. Sadrže ADP, Ca2+, serotonin, fosfolipide, enzime sinteze prostaglandina i tromboksana, trombostenin (poput mišićnog aktomiozina osigurava kontraktilnu sposobnost ovih stanica), trombogeni faktor rasta epitela i mišićnih stanica vaskularne stijenke te niz drugih tvari. Humoralna regulacija funkcija trombocita provodi se putem specijaliziranih receptora njihovih membrana (alfa2- i beta2-adrenoreceptori, receptori za histamin i serotonin, acetilkolin, tromboksan, adenozin i niz drugih). Posebno svojstvo trombocita je visok afinitet za kolagen i druge subendotelne elemente vaskularne stijenke, za površine koje se ne kvaše i negativno nabijene. Ovo svojstvo trombocitima pruža iznimnu sposobnost prianjanja (lijepljenja) na dio žile s oštećenim endotelom, koji ima velike mogućnosti oštećenja tijekom šoka. U tom slučaju, trombociti se šire i oslobađaju pseudopodije, koje se mogu prilijepiti jedna za drugu i za stijenku krvne žile. Propusnost membrane se povećava, a ADP, serotonin, tromboksan i neki faktori koagulacije adsorbirani na površini trombocita oslobađaju se iz trombocita. Te tvari stupaju u interakciju s odgovarajućim receptorima na membrani i, uz sudjelovanje kalcijevih iona, uzrokuju agregaciju (u početku reverzibilnu). Proces postaje samoodrživ, što je olakšano humoralnim regulatornim čimbenicima; drugi čimbenici, naprotiv, mogu ga zaustaviti, pa čak i preokrenuti, uzrokujući deagregaciju.
S prevladavanjem utjecaja i uvjeta koji stvaraju trombe, faze adhezije i reverzibilne agregacije zamjenjuju se trećom fazom - ireverzibilnom agregacijom, koja se provodi uz sudjelovanje trombostenina i dovodi do suženja ugruška; reakcija jačanja agreganta i suženja također se događa uz sudjelovanje Ca+, ATP-a i dovodi do stvaranja bijelog tromba.
Ciklooksigenazni put pretvorbe arahidonske kiseline u trombocitima, vaskularnim endotelnim stanicama i drugim tkivima osigurava lokalnu (poluvrijeme raspada metabolita je vrlo kratko) homeostazu koagulacije, budući da se tijekom ovog metabolizma stvaraju snažne pro- i antiagregacijske tvari. Glavni faktor koji aktivira agregaciju trombocita u lancu reakcija ciklooksigenaze je tromboksan A2, a njegov ne manje snažan antagonist je prostaciklin, koji proizvode endotelne stanice i, u manjoj mjeri, prostaglandini serije E i G. Konačno, na agregaciju trombocita snažno utječu dodatni lokalni i sistemski humoralni čimbenici.
Aktivatori i inhibitori agregacije trombocita
Inicijatori i aktivatori agregacije trombocita |
Inhibitori agregacije trombocita |
Kolagen |
- |
ADP |
Adenozin i njegovi stabilizatori |
Norepinefrin (putem alfa2 receptora) |
Alfa-adrenergički blokatori |
Serotonin |
Antiserotoninski agensi |
Histamin |
Antihistaminici |
Trombin |
Heparin |
Ca2+ |
Antagonisti Ca2+ |
CGMP - njegovi induktori (acetilkolin?) i stabilizatori |
CAM - njegovi induktori (putem beta-adrenergičkih receptora) i stabilizatori (inhibitori fosfodiesteraze) |
Arahidonska kiselina |
Dekstrani, albumin |
Tromboksan A2 |
Prostaciklin I2 |
Farmakološke intervencije u početnoj fazi stvaranja tromba u šoku i akutnim ishemijskim procesima u srcu i mozgu ukazuju na sljedeću mogućnost:
- inhibicija početnih reakcija (potpunih i djelomičnih) kaskade arahidonske kiseline;
- inhibicija određene reakcije sinteze tromboksana;
- blokada receptora za leukotriene i tromboksane u trombocitima, glatkim mišićima i drugim stanicama;
- upotreba tvari koje moduliraju agregaciju trombocita, tj. na druge načine slabe reakciju potonje na utjecaj inicijacijskih čimbenika (kolagen, tromboksan A2, leukotrieni itd.).
Provedba navedenih načina korekcije poremećaja reoloških svojstava krvi omogućuje rješavanje glavnog taktičkog zadatka: zaštititi receptore agregacije i adhezije trombocita od učinka aktivatora ili suzbiti unutarstanične mehanizme sinteze tih receptora. Inhibicija početnih reakcija kaskade arahidonske kiseline može se postići zaštitom receptora trombocita koji reagiraju na polimerne aktivatore, korištenjem niskomolekularnih dekstrana, čije se molekule natječu s fibrinom, kolagenom, agregiranim imunoglobulinom (IgE) i komponentama sustava komplementa.
Maskiranjem receptora na membrani trombocita i natjecanjem s proteinima s velikom disperzijom na površini eritrocita, niskomolekularni dekstrani ih istiskuju i uništavaju mostove između stanica. To je zbog činjenice da dekstrani, obavijajući vaskularni endotel i površinu staničnih elemenata krvi, povećavaju njihov negativni naboj, čime pojačavaju antiagregacijska svojstva.
Dekstrani
Dekstrani niske molekularne težine smanjuju agregaciju trombocita induciranu kolagenom i ADP-om, kao i aktivirajući učinak trombina na trombocite, inhibiraju rast početnog bijelog trombocitnog tromba, poboljšavaju protok krvi, smanjuju postoperativni porast sadržaja fibrinogena u plazmi te mijenjaju strukturu i stabilnost fibrina.
Intravenske infuzije dekstrana kod traume i šoka ne samo da smanjuju agregaciju i adheziju trombocita, već i mobiliziraju endogeni heparin, čime potiču stvaranje labavog i slabo retraktibilnog krvnog ugruška, koji se lako lizira fibrinoliticima. Antitrombinska aktivnost niskomolekularnih dekstrana povezana je s njihovim specifičnim učinkom na strukturu i funkciju faktora koagulacije krvi VIII. Faktor VIII (antihemofilni globulin), velika molekula sa složenom strukturom i funkcijom, uključen je u agregaciju trombocita i stabilnost nastalog ugruška. Dekstrani ometaju djelovanje faktora VIII, čime usporavaju agregaciju trombocita i smanjuju stabilnost ugruška.
Dekstrani niske molekularne težine nisu pravi antikoagulansi i njihov korektivni učinak kod hemoreoloških poremećaja povezan je uglavnom s hemodilucijom, nadoknadom volumena cirkulirajuće plazme i poboljšanjem protoka krvi u mikrocirkulacijskom sustavu.
Sposobnost dekstrana da poboljšaju protok krvi kod hemodinamskih poremećaja (šok, gubitak krvi) posljedica je kompleksa čimbenika. Pojava visoke prolazne koncentracije polimera u krvi ne samo da dovodi do "izravne hemodilucije", već stvara i uvjete za protok tekućine u krvotok iz intersticijskog prostora i naknadno uravnoteženje osmotskog učinka dekstrana. Kao posljedica hemodilucije, smanjuje se viskoznost krvi, povećava se venski dotok u srce i povećava se minutni volumen srca. Uz te učinke, dekstrani tvore komplekse s fibrinogenom i imaju antilipemijski učinak.
Dakle, antiagregacijsko djelovanje i hemodinamski učinci niskomolekularnih dekstrana pomažu u smanjenju viskoznosti krvi, što je posebno važno pri niskim brzinama smicanja. Dezagregacija krvnih stanica poboljšava sistemski protok krvi i mikrocirkulaciju, posebno u njezinom venskom dijelu, gdje su gradijenti brzine najniži. Primjena otopina niskomolekularnog dekstrana kod različitih vrsta šoka, tijekom kirurškog liječenja ozljeda i njihovih posljedica, a zatim u postoperativnom razdoblju pomaže u sprječavanju hiperkoagulacije i smanjenju vjerojatnosti trombotičkih procesa i embolije.
Međutim, treba napomenuti da su u nekim slučajevima infuzije otopina dekstrana popraćene anafilaktičkim i alergijskim reakcijama (opasno u prisutnosti senzibilizacije i anafilaktičkog šoka). To je zbog činjenice da dekstrani, koji imaju veliku molekularnu težinu i mnogo bočnih lanaca, mogu djelovati kao antigen. Stoga se, kako bi se utvrdila individualna osjetljivost, preporučuje prethodna intravenska primjena do 20 ml otopine dekstrana niske molekularne težine kao haptena (15%-tna otopina, molekularna težina 1000) i provođenje infuzija nadomjesnog plazma preparata prije uvođenja anestezije.
 [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ]
[ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ]
Inhibitori trombina
Farmakološka zaštita receptora trombocita koji stupaju u interakciju s aktivatorima trombocita može se postići i korištenjem sredstava koja se natječu s nepolimernim aktivatorima trombocita ili ih inhibiraju. Takva sredstva uključuju inhibitore trombina (heparin i hirudin, niz sintetskih inhibitora, antagoniste adrenalina), blokatore alfa-receptora (fentolamin, dihidroergotamin), antagoniste ADP-a (dipiridamol, adenozin i njegovi strukturni analozi, fosfokreatin), antagoniste serotonina (metisergid). Samo nekoliko navedenih sredstava zapravo se koristi za prevenciju i terapiju šoka različitog podrijetla.
Zaštita unutarstaničnih mehanizama sinteze proteinskih receptora koji reagiraju s aktivatorima agregacije i adhezije trombocita, te inhibicija procesa sinteze tromboksana mogući su lijekovima različitih skupina:
- induktori i stabilizatori cATP-a, prostaciklina i prostaglandina PgE2;
- inhibitori fosfolipaze i fosfodiesteraze.
Intenzivan razvoj posebnih antitrombocitnih sredstava započeo je relativno nedavno i još nije doveo do pouzdanih rezultata. Trenutno se u kliničkoj praksi, osim otopina dekstrana, široko koriste antitrombocitna sredstva poput acetilsalicilne kiseline, indometacina, dipiradamola, sulfinpirazona (persantina), prostaciklina (eikoprostenon) i heparina za sprječavanje stvaranja bijelih trombocita.
Nesteroidni protuupalni lijekovi
Utvrđeno je da su farmakološki učinci nesteroidnih protuupalnih lijekova - acetilsalicilne kiseline i indometacina - posljedica njihovog utjecaja na metabolizam eikozanoida (tromboksana i prostaglandina). Gotovo svi lijekovi u ovoj skupini inhibiraju enzimski kompleks poznat kao prostaglandin sintetaza, čime ostvaruju svoje specifične i antiagregacijske učinke.
Acetilsalicilna kiselina se vrlo brzo apsorbira nakon oralne primjene. Produkt njezine hidrolize, salicilna kiselina, uzrokuje inhibiciju trombocitne ciklooksigenaze, što remeti pretvorbu arahidonske kiseline u prostaglandin O2 i, u konačnici, tromboksan A2. Acetilsalicilna kiselina inhibira agregaciju induciranu kolagenom, ADP-om, adrenalinom i serotoninom. Iako je njezina GG05 vrijednost 15 minuta, antiagregacijski učinak traje nekoliko dana, što se očito objašnjava ireverzibilnom inhibicijom reakcija sinteze prostaglandina i supresijom funkcije agregacije trombocita tijekom cijelog njihovog životnog vijeka (6-10 dana). Uz inhibiciju trombocitne ciklooksigenaze, acetilsalicilna kiselina u visokim dozama inhibira ciklooksigenazu vaskularne stijenke i istovremeno sa supresijom sinteze tromboksana A2 inhibira sintezu prostaciklina u endotelnim stanicama. Stoga se acetilsalicilna kiselina treba propisivati kao antiagregacijski lijek u malim dozama (3000-5000 mg/dan), koje pretežno inhibiraju agregaciju trombocita.
S obzirom na to da acetilsalicilna kiselina blokira trombocitnu ciklooksigenazu nekoliko dana, a endotelnu ciklooksigenazu ne više od jednog dana, racionalno je propisivati lijek ne svakodnevno, već svaka 3-4 dana. Odabir optimalne doze acetilsalicilne kiseline za pacijenta treba provoditi individualno, budući da postoji različita osjetljivost pacijenata na antitrombocitni učinak lijeka. Kod reaktivnih pacijenata, acetilsalicilna kiselina u dozi od 0,5 g inhibira agregaciju trombocita za 40-50%, kod hiperreaktivnih pacijenata - potpuno ili za 80-90%, a za areaktivne pacijente karakteristična je odsutnost antitrombocitnog učinka pri uzimanju iste doze lijeka.
Selektivni inhibitori tromboksan sintetaze su imidazol i njegovi analozi, koji ne blokiraju ciklooksigenazu. Dipiridamol, koji se u kliničkoj praksi koristi u liječenju kronične ishemijske bolesti srca kao koronarni dilatator, poput imidazola selektivno inhibira tromboksan sintetazu, sprječavajući sintezu tromboksana A2. Vjeruje se da lijek i njegovi analozi također inhibiraju trombocitnu fosfodiesterazu, čime povećavaju koncentraciju cAMP-a u trombocitima. Uz to, dipiridamol inhibira aktivnost adenozin deaminaze i unos adenozina od strane trombocita, blokira apsorpciju serotonina od strane trombocita i njihovu agregaciju induciranu adrenalinom i kolagenom. Postoje izvješća o slaboj antitrombocitnoj aktivnosti lijeka i njegovoj sposobnosti da u malim dozama pojača agregaciju trombocita. Najpouzdaniji antitrombocitni učinak može se postići kombinacijom dipiridamola i acetilsalicilne kiseline.
Heparin
Među antitrombotskim sredstvima, jedan od najučinkovitijih regulatora agregatnog stanja krvi je heparin, posebno kada se koristi rano. Heparin ima visoki negativni naboj i sposoban je za interakciju s velikim i malim ionima i molekulama (enzimi, hormoni, biogeni amini, proteini plazme itd.), pa je spektar njegovog biološkog djelovanja prilično širok. Lijek ima antitrombinske, antitromboplastinske i antiprotrombinske učinke, sprječava pretvorbu fibrinogena u fibrin, potiskuje retrakciju ugruška i povećava fibrinolizu.
Mehanizam antikoagulantnog djelovanja heparina je prilično složen. Sada je utvrđeno da su antikoagulantni učinci heparina povezani s pojačavanjem djelovanja antitrombina III i povećanjem sposobnosti kompleksa heparin-antitrombin III da brzo inaktivira većinu serinskih proteaza sustava koagulacije krvi. U antitrombotskom učinku heparina, od velike je važnosti njegova sposobnost povećanja i održavanja visokog elektronegativnog potencijala vaskularne intime, sprječavajući adheziju trombocita i stvaranje trombocitnih mikrotromba. Heparin najaktivnije suzbija stvaranje tromba u venama, sprječavajući i lokalno stvaranje tromba i diseminiranu intravaskularnu koagulaciju.
Prostaciklin i njegovi stabilni analozi
Među antitrombocitnim sredstvima, najsnažniji inhibitori agregacije su prostaciklin i njegovi stabilni analozi. Antitrombocitni učinak prostaciklina posljedica je stimulacije adenilat ciklaze i, kao posljedica toga, povećanja koncentracije cAMP-a u trombocitima, smanjenja sadržaja tromboksana, smanjenja sadržaja tromboksana A2 i blokade njegovih receptora. Prostaciklin je nestabilan i brzo se hidrolizira do neaktivnih produkata, pa se primjenjuje intravenski kapanjem brzinom od 2 do 20 ng/kg u minuti tijekom 30-60 minuta do 6 puta dnevno.
Prostaciklin, uz snažan antiagregacijski učinak, ima snažan vazodilatacijski i bronhodilatacijski učinak. Lijek širi krvne žile mozga, srca, bubrega, skeletnih mišića i mezenteričnih krvnih žila. Pod utjecajem prostaciklina povećava se koronarni protok krvi, povećava se opskrba miokarda energijom i smanjuje se njegova potreba za kisikom. Unatoč njegovoj nestabilnosti u tijelu, klinički povoljni učinci mogu trajati nekoliko tjedana, pa čak i mjeseci. Mehanizam takvog produljenog djelovanja još nije jasan.
Prostaciklin je niskotoksičan lijek, ali njegova primjena može uzrokovati nuspojave: crvenilo lica, glavobolje, snižen krvni tlak, bol u trbuhu, anoreksiju. Uz prostaciklin, njegovi sintetski stabilni analozi (iloprost itd.) obećavajući su inhibitori agregacije trombocita.
Lijekovi koji poboljšavaju viskoznost krvi
Poremećaji reoloških svojstava krvi tijekom traume i šoka uzrokovani su ne samo promjenama funkcionalne aktivnosti trombocita, već i povećanjem viskoznosti krvi. Strukturna viskoznost krvi kao složenog dinamičkog dispergiranog sustava uvelike je određena viskoznošću plazme i sposobnošću eritrocita da se deformiraju. Viskoznost plazme uglavnom ovisi o koncentraciji proteina u krvi. Proteini male molekularne težine, poput albumina, imaju mali utjecaj na viskoznost plazme, dok proteini velike molekule (fibrinogen, alfa- i gama-globulini, druge makromolekule) značajno je povećavaju.
Pri niskim brzinama smicanja, adsorpcija fibrinogena i globulina na površini eritrocita dovodi do stvaranja mostova između susjednih stanica i stvaranja agregata iz eritrocita. Brzina stvaranja agregata je složen biofizički proces i ovisi ne samo o veličini smicanja, već i o elektrokinetičkim svojstvima eritrocita, koncentraciji, masi i sorpcijskom kapacitetu makromolekula-agregatora, o obliku i plastičnosti eritrocita.
Održavanje oblika i mehaničkih svojstava membrane eritrocita zahtijeva značajan utrošak energije. Smatra se da se energija proizvedena u eritrocitima tijekom glikolize troši na fosforilaciju spektrina, što rezultira promjenama u sekundarnoj strukturi proteina i interakcijom sa susjednim komponentama unutarnje membrane. Interakcija između strukturnih proteina membrane, spektrina i aktina, igra važnu ulogu u formiranju mehaničkih svojstava membrane eritrocita, u održavanju konstantne površine eritrocita i njegove debljine pri bilo kojoj deformaciji.
U slučaju sistemskih hemodinamskih i organskih poremećaja protoka krvi, povećanje krutosti eritrocitnih membrana i stvaranje eritrocitnih agregata dovodi do smanjenja brzine prolaska eritrocita kroz kapilare, čime se narušava funkcija prijenosa plinova u krvi. Stoga bi korekcija poremećaja reoloških svojstava krvi u šoku trebala uključivati, uz sprječavanje agregacije eritrocita, normalizaciju viskoznosti plazme i krvi, agregaciju i deformaciju eritrocita.
Uz niskomolekularne dekstrane, otopine albumina jedno su od učinkovitih sredstava za povećanje stabilnosti suspenzije krvi. U kasnom razdoblju šoka dolazi do generalizirane agregacije eritrocita na pozadini smanjenja koncentracije albumina u krvnoj plazmi i povećanja koncentracije fibrinogena i globulina, posebno alfa2 frakcije, lipoproteina i lipida. U tim uvjetima, reološki učinci albumina posljedica su dva glavna čimbenika: hemodilucije i normalizacije omjera između mikro- i makroglobularnih proteina u plazmi. Istodobno, albumin veže slobodne kiseline, čija labilizacija tijekom traume i šoka potiče agregaciju staničnih struktura krvi i intravaskularnu koagulaciju te može uzrokovati masnu emboliju.
Mjere protiv šoka usmjerene na nadoknađivanje volumena cirkulirajuće krvi, uklanjanje hipoksije tkiva i metaboličke acidoze, doprinose normalizaciji elastičnosti membrana eritrocita, budući da hipoksija i acidoza značajno smanjuju deformabilnost eritrocita. Povećana krutost membrana eritrocita u šoku vjerojatno je povezana s inhibicijom sinteze ATP-a u eritrocitima. Zauzvrat, smanjenje koncentracije ATP-a doprinosi povećanju koncentracije Ca2+ u eritrocitima, koji, vezanjem na membranske proteine, povećava krutost membrane.
Jedan od farmakoloških lijekova koji povećava sadržaj ATP-a u eritrocitima i elastičnost membrana eritrocita je Trental (pentoksifilin), koji se u kliničkoj praksi koristi za liječenje ishemijskih poremećaja.
Uz smanjenje krutosti membrana eritrocita, Trental uzrokuje vazodilataciju, poboljšava oksigenaciju tkiva, inhibira aktivnost fosfodiesteraze u tkivima, povećava koncentraciju cAMP-a i inhibira agregaciju trombocita.
Među ostalim farmakološkim sredstvima koja održavaju elastičnost membrane eritrocita, vrijedi istaknuti antagoniste Ca2+, koji ograničavaju protok iona u eritrocite (flunarizin, nifedipin itd.).
 [ 19 ], [ 20 ], [ 21 ], [ 22 ], [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ]
[ 19 ], [ 20 ], [ 21 ], [ 22 ], [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ]
Pažnja!
Da bi se pojednostavnila percepcija informacija, ova uputa za upotrebu lijeka "Lijekovi koji sprječavaju trombozu i poboljšavaju reološke karakteristike krvi" prevedena je i predstavljena u posebnom obliku na temelju službenih uputa za medicinsku uporabu lijeka. Prije upotrebe pročitajte napomenu koja je došla izravno na lijek.
Opis je predviđen za informativne svrhe i nije vodič samoizlječenja. Potreba za ovim lijekom, svrha režima liječenja, metode i dozu lijeka određuje isključivo liječnik. Samo-lijek je opasan za vaše zdravlje.

